SARS-CoV-2/Influenza A/Influenza B
Produktname
HWTS-RT148-SARS-CoV-2/Influenza A/Influenza B Nukleinsäure-Kombinationsnachweiskit (Fluoreszenz-PCR)
Kanal
| Kanalname | PCR-Mix 1 | PCR-Mix 2 |
| FAM-Kanal | ORF1ab-Gen | USt-IdNr. |
| VIC/HEX-Kanal | Interne Kontrolle | Interne Kontrolle |
| CY5-Kanal | N-Gen | / |
| ROX-Kanal | E-Gen | IVB |
Technische Parameter
| Lagerung | -18℃ |
| Haltbarkeit | 12 Monate |
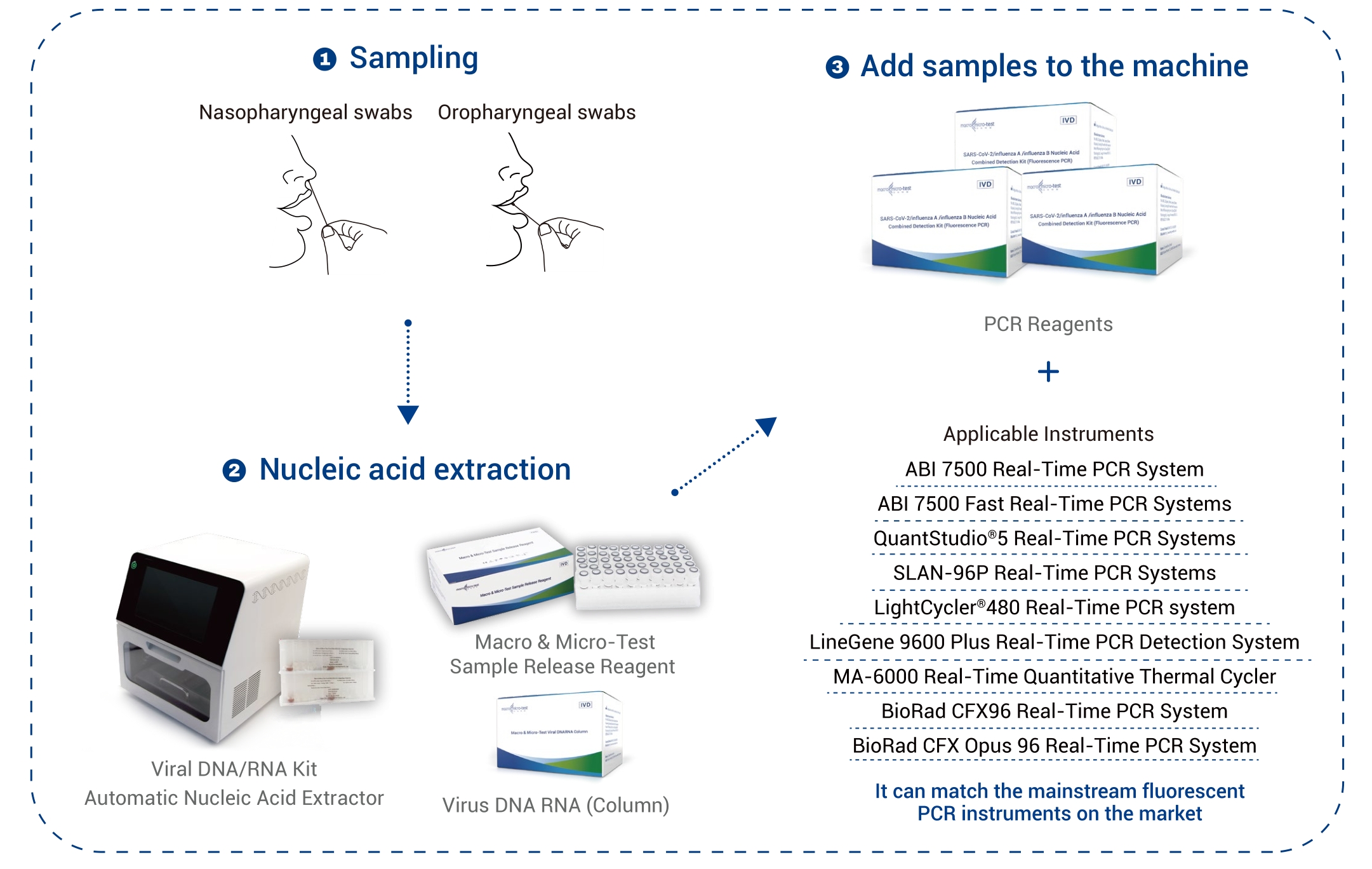
| Probenart | Nasen-Rachen-Abstriche und Rachen-Abstriche |
| Ziel | SARS-CoV-2 drei Zielstrukturen (Orf1ab-, N- und E-Gene)/Influenza A/Influenza B |
| Ct | ≤38 |
| CV | ≤10,0 % |
| LoD | SARS-CoV-2: 300 Kopien/ml Influenza-A-Virus: 500 Kopien/ml Influenza-B-Virus: 500 Kopien/ml |
| Spezifität | a) Die Ergebnisse der Kreuztests zeigten, dass das Kit mit folgenden humanen Coronaviren kompatibel war: SARSr-CoV, MERSr-CoV, HCoV-OC43, HCoV-229E, HCoV-HKU1, HCoV-NL63, Respiratorisches Synzytialvirus A und B, Parainfluenzavirus 1, 2 und 3, Rhinovirus A, B und C, Adenovirus 1, 2, 3, 4, 5, 7 und 55, Humanes Metapneumovirus, Enterovirus A, B, C und D, Humanes Zytoplasma-Pulmonalvirus, Epstein-Barr-Virus, Masernvirus, Humanes Zytomegalievirus, Rotavirus, Norovirus, Mumpsvirus, Varicella-Zoster-Virus, Mycoplasma pneumoniae, Chlamydia pneumoniae, Legionella, Pertussis, Haemophilus influenzae, Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes, Klebsiella pneumoniae, Mycobacterium tuberculosis, Aspergillus fumigatus, Candida albicans, Candida glabrata Es gab keine Kreuzreaktion zwischen Pneumocystis yersini und Cryptococcus neoformans. b) Antiinterferenzfähigkeit: Ausgewähltes Mucin (60 mg/ml), 10 % (V/V) Humanblut, Diphenylephrin (2 mg/ml), Hydroxymethylzolin (2 mg/ml), Natriumchlorid (mit Konservierungsmittel) (20 mg/ml), Beclomethason (20 mg/ml), Dexamethason (20 mg/ml), Flunison (20 μg/ml), Triamcinolonacetonid (2 mg/ml), Budesonid (2 mg/ml), Mometason (2 mg/ml), Fluticason (2 mg/ml), Histaminhydrochlorid (5 mg/ml), α-Interferon (800 IE/ml), Zanamivir (20 mg/ml), Ribavirin (10 mg/ml), Oseltamivir (60 ng/ml), Pramivir (1 mg/ml), Lopinavir (500 mg/ml), Ritonavir (60 mg/ml), Mupirocin (20 mg/ml), Azithromycin (1 mg/ml), Ceproten (40 μg/ml), Meropenem (200 mg/ml), Levofloxacin (10 μg/ml) und Tobramycin (0,6 mg/ml). Die Ergebnisse zeigten, dass die Störsubstanzen in den genannten Konzentrationen die Nachweisergebnisse der Krankheitserreger nicht beeinflussten. |
| Anwendbare Instrumente | Applied Biosystems 7500 Echtzeit-PCR-Systeme Applied Biosystems 7500 Fast Real-Time PCR-Systeme SLAN ®-96P Echtzeit-PCR-Systeme QuantStudio™ 5 Echtzeit-PCR-Systeme LightCycler®480 Echtzeit-PCR-System LineGene 9600 Plus Echtzeit-PCR-Detektionssystem MA-6000 Echtzeit-Quantitativer Thermocycler BioRad CFX96 Echtzeit-PCR-System BioRad CFX Opus 96 Echtzeit-PCR-System |
Gesamt-PCR-Lösung