Nukleinsäure- und Rifampicinresistenz von Mycobacterium tuberculosis
Produktname
HWTS-RT074B-Mycobacterium Tuberculosis Nukleinsäure- und Rifampicin-Resistenz-Nachweiskit (Schmelzkurve)
Zertifikat
CE
Epidemiologie
Mycobacterium tuberculosis, kurz Tuberkelbakterium (TB), ist das pathogene Bakterium, das Tuberkulose verursacht. Zu den gängigen Tuberkulosemedikamenten der ersten Wahl gehören Isoniazid, Rifampicin und Hexambutol. Zu den Medikamenten der zweiten Wahl zählen Fluorchinolone, Amikacin und Kanamycin. Neu entwickelte Medikamente sind Linezolid, Bedaquilin und Delamani. Aufgrund unsachgemäßer Anwendung von Tuberkulosemedikamenten und der besonderen Zellwandstruktur von Mycobacterium tuberculosis entwickelt das Bakterium jedoch Resistenzen gegen diese Medikamente. Dies stellt eine ernsthafte Herausforderung für die Prävention und Behandlung von Tuberkulose dar.
Rifampicin wird seit den späten 1970er Jahren häufig zur Behandlung von Lungentuberkulose eingesetzt und zeigt eine signifikante Wirkung. Es gilt als Mittel der ersten Wahl zur Verkürzung der Chemotherapie bei Lungentuberkulose. Rifampicin-Resistenzen werden hauptsächlich durch Mutationen des rpoB-Gens verursacht. Obwohl ständig neue Tuberkulosemedikamente entwickelt werden und sich die klinische Wirksamkeit bei Lungentuberkulose stetig verbessert, besteht weiterhin ein Mangel an wirksamen Tuberkulosemedikamenten, und der unsachgemäße Gebrauch von Medikamenten ist in der Klinik relativ häufig. Offensichtlich können Mycobacterium tuberculosis bei Patienten mit Lungentuberkulose nicht vollständig und rechtzeitig abgetötet werden, was letztendlich zu unterschiedlich starker Arzneimittelresistenz im Körper des Patienten führt, den Krankheitsverlauf verlängert und das Sterberisiko erhöht.
Kanal
| Kanal | Kanäle und Fluorophore | Reaktionspuffer A | Reaktionspuffer B | Reaktionspuffer C |
| FAM-Kanal | Reporter: FAM, Quencher: Keine | rpoB 507-514 | rpoB 513-520 | 38KD und IS6110 |
| CY5-Kanal | Reporter: CY5, Quencher: Keine | rpoB 520-527 | rpoB 527-533 | / |
| HEX (VIC) Kanal | Reporter: HEX (VIC), Quencher: Keine | Interne Kontrolle | Interne Kontrolle | Interne Kontrolle |
Technische Parameter
| Lagerung | ≤-18℃ Im Dunkeln |
| Haltbarkeit | 12 Monate |
| Probenart | Sputum |
| CV | ≤5,0 % |
| LoD | Mycobacterium tuberculosis 50 Bakterien/ml Rifampicin-resistenter Wildtyp: 2x103Bakterien/ml homozygoter Mutant: 2x103Bakterien/ml |
| Spezifität | Es erkennt Wildtyp-Mycobacterium tuberculosis und die Mutationsstellen anderer Arzneimittelresistenzgene wie katG 315G>C\A, InhA-15C>T. Die Testergebnisse zeigen keine Resistenz gegen Rifampicin, was bedeutet, dass keine Kreuzreaktivität vorliegt. |
| Anwendbare Instrumente: | SLAN-96P Echtzeit-PCR-Systeme BioRad CFX96 Echtzeit-PCR-System LightCycler480® Echtzeit-PCR-System |
Arbeitsablauf
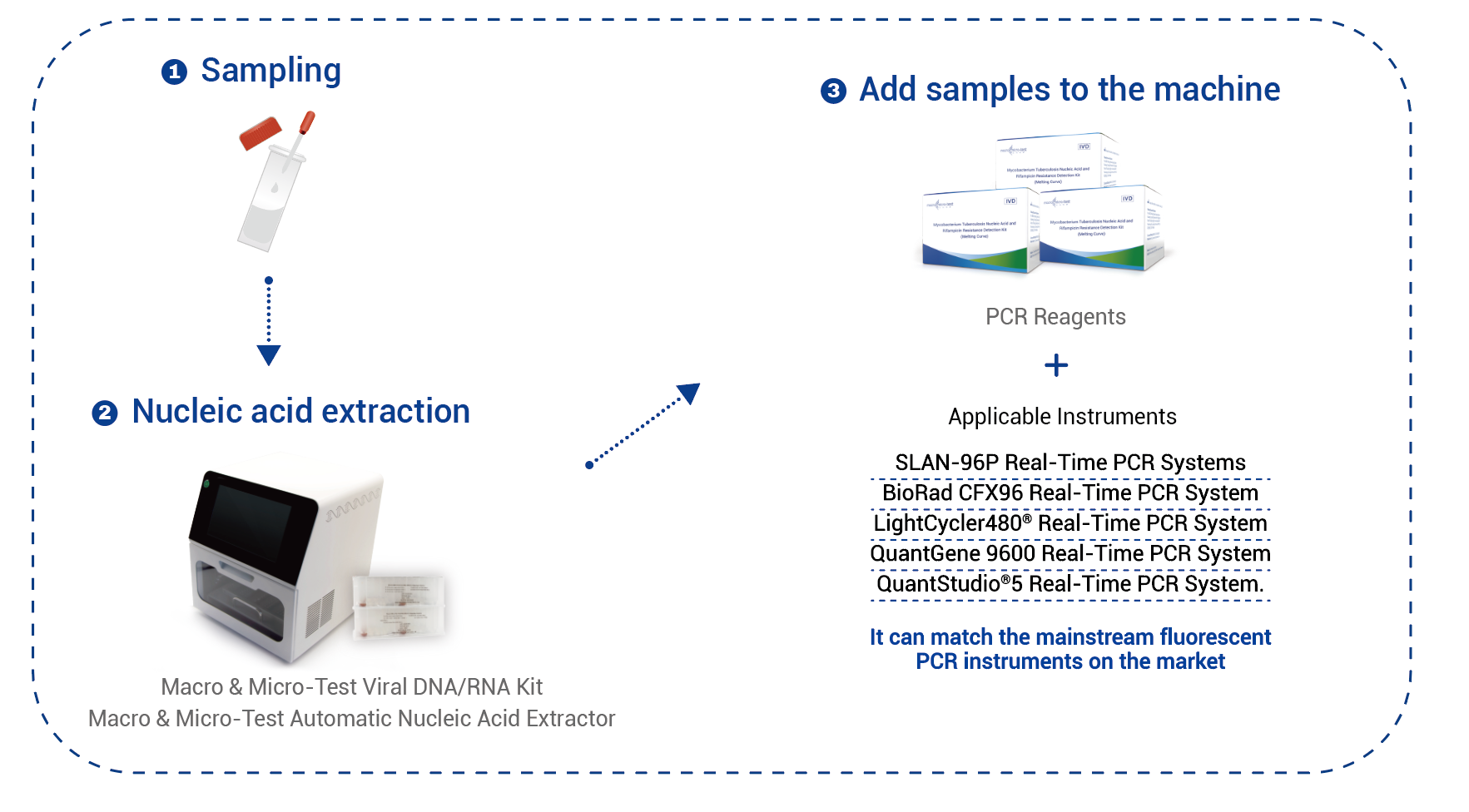
Bei Verwendung des Macro & Micro-Test General DNA/RNA Kits (HWTS-3019-50, HWTS-3019-32, HWTS-3019-48, HWTS-3019-96) (das mit dem Macro & Micro-Test Automatic Nucleic Acid Extractor (HWTS-3006C, HWTS-3006B) verwendet werden kann) oder der Macro & Micro-Test Viral DNA/RNA Column (HWTS-3022-50) von Jiangsu Macro & Micro-Test Med-Tech Co., Ltd. zur Extraktion werden nacheinander 200 μL der Positivkontrolle, der Negativkontrolle und der zu testenden aufbereiteten Sputumprobe hinzugegeben. Zusätzlich werden jeweils 10 μL der internen Kontrolle zu jeder Probe hinzugefügt. Die weiteren Schritte sind strikt gemäß der Extraktionsanleitung durchzuführen. Das extrahierte Probenvolumen beträgt 200 μL, das empfohlene Elutionsvolumen beträgt 100 μL.