I. Überblick über dieESMOLeitlinie 2025
Im August 2025 veröffentlichte die ESMO offiziell die Leitlinie „ESMO Clinical Practice Guideline for diagnosis, treatment and follow up“ für nicht-kleinzelligen Lungenkrebs im Früh- und lokal fortgeschrittenen Stadium. Die Publikation erschien in der renommierten onkologischen Fachzeitschrift „Annals of Oncology“. Dies ist die erste umfassende Aktualisierung seit der Version von 2017 und bietet Onkologen weltweit eine äußerst maßgebliche Referenz.

Lungenkrebs weist weltweit die höchste Inzidenz und Mortalität aller Krebserkrankungen auf. Jedes Jahr gibt es mehr als 2,2 Millionen Neuerkrankungen und über 1,8 Millionen Todesfälle, was Lungenkrebs zur häufigsten krebsbedingten Todesursache bei Männern und Frauen macht. Nicht-kleinzelliger Lungenkrebs (NSCLC) betrifft etwa 80–85 % aller Lungenkrebsfälle. Vor diesem Hintergrund bringt die Veröffentlichung der Leitlinie 2025 neue wissenschaftliche Impulse in die klinische Praxis, wobei die Aktualisierung der Biomarker-Teststrategien von besonderer Bedeutung ist.
II. Auslegung wichtiger Aktualisierungen der Leitlinien
2.1 Biomarker-Tests: Von „optional“ zu „essenziell“
Die Leitlinie von 2025 stellt eine wegweisende strategische Anpassung hinsichtlich der Biomarker-Testung dar. Sie stellt ausdrücklich fest, dass die Biomarker-Testung für die Behandlungsentscheidung bei Patienten mit NSCLC im Stadium IB-III unerlässlich ist.
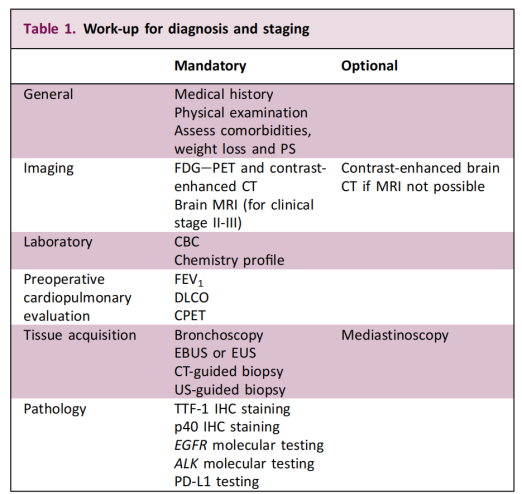
Diese Empfehlung erweitert die molekulare Diagnostik von ihrem bisherigen Fokus auf Patienten mit fortgeschrittener Erkrankung auf resektable Fälle im Frühstadium. Hauptziel ist die Identifizierung treibender Genmutationen und die Schaffung einer wissenschaftlichen Grundlage für eine personalisierte Präzisionstherapie. Die Leitlinie betont zudem, dass die Durchführbarkeit einer Biopsie und das diagnostische Vorgehen von einem multidisziplinären Team anhand der Patienten- und Tumoreigenschaften festgelegt werden sollten.
Bezüglich der spezifischen Teststrategie empfiehlt die Leitlinie eindeutig, Gentests vor der chirurgischen Entscheidung durchzuführen und diese mindestens auf EGFR und ALK abzudecken. Dieses Konzept der „vorzeitigen Testung“ ist von großer klinischer Bedeutung für die präzise Stratifizierung und personalisierte Behandlung von NSCLC im Frühstadium – die Aktualität und Genauigkeit der Testergebnisse bestimmen unmittelbar die Wahl der nachfolgenden adjuvanten Therapie.
2.2 Therapeutische Durchbrüche bei NSCLC im Frühstadium mit positivem Treiberonkogen.
Die Leitlinie 2025 integriert Erkenntnisse aus mehreren großen klinischen Studien, um einen klaren Behandlungspfad für Patienten mit NSCLC im Frühstadium mit positivem Treiberonkogen zu etablieren.
EGFR-mutierte positive Patienten:Basierend auf der wegweisenden ADAURA-Studie hat sich die postoperative adjuvante Osimertinib-Therapie über drei Jahre weltweit als Standardtherapie für Patienten mit EGFR-Exon-19-Deletionen oder Exon-21-L858R-Mutationen etabliert. Die ADAURA-Studie ist eine internationale, multizentrische, randomisierte, kontrollierte Phase-III-Studie zur Bewertung der Wirksamkeit und Sicherheit von adjuvantem Osimertinib bei Patienten mit vollständig reseziertem, EGFR-mutiertem NSCLC im Stadium IB-IIIA. Die Studie zeigte, dass Osimertinib sowohl das krankheitsfreie Überleben als auch das Gesamtüberleben im Vergleich zu Placebo signifikant verbesserte und sich damit als neuer Therapiestandard für diese Patientengruppe etablierte. Explorative Analysen der ADAURA-Studie ergaben jedoch, dass etwa 36 % der Therapieabbrüche auf Nebenwirkungen und weitere 31 % auf die Entscheidung der Patienten zurückzuführen waren. Dieser Befund unterstreicht die Notwendigkeit einer präzisen Ausgangsdiagnostik vor Behandlungsbeginn, um sicherzustellen, dass die zielgerichtete Therapie nur Patienten verabreicht wird, die einen nachhaltigen Nutzen daraus ziehen können.
ALK-positive Patienten:Basierend auf der ALINA-Studie gilt die postoperative adjuvante Therapie mit Alectinib über zwei Jahre nun als Standard. In der Primäranalyse der randomisierten, offenen Phase-III-Studie ALINA zeigte Alectinib einen deutlichen Vorteil im krankheitsfreien Überleben (DFS) bei Patienten im Stadium II–IIIA (Hazard Ratio 0,24). Aktualisierte Daten der ALINA-Studie, die auf dem ESMO-Kongress 2025 präsentiert wurden, belegten, dass der DFS-Vorteil von Alectinib nach mindestens drei Jahren Nachbeobachtung weiterhin „anhaltend und klinisch relevant“ war (Hazard Ratio 0,36) bei Patienten im Stadium II–IIIA. Die zuletzt berichtete 4-Jahres-Gesamtüberlebensrate lag bei 98,4 %, die 4-Jahres-DFS-Rate bei 75,5 %. Auch das DFS im zentralen Nervensystem war verbessert, ohne dass neue Sicherheitssignale auftraten. Diese aussagekräftigen Daten festigen die adjuvante Therapie mit Alectinib als Standard nach Resektion von ALK-positivem NSCLC und unterstreichen die Bedeutung präziser Tests zur Identifizierung dieser Patienten.
Wahl der Testmethode:Die ESMO-Leitlinie 2025 listet explizit aufMultiplex-RT-PCR-Panel-AssaysNeben RNA-basierter NGS, IHC und FISH als einer der empfohlenen technischen Ansätze zum Nachweis von ALK-Fusionen zeigt die Leitlinie, dass ihre Kernanforderung darin besteht, Tests zur Unterstützung klinischer Entscheidungen durchzuführen, anstatt eine bestimmte Testplattform vorzuschreiben. Für RT-PCR-Produkte zum Nachweis von EGFR und ALK liefert diese flexible Teststrategie eine starke, leitlinienbasierte Begründung für deren Einsatz in der klinischen Praxis.
III. Technische Lösungen für Präzisionsprüfungen
Die Leitlinie von 2025 sieht vor, die Testung bereits in die präoperative Entscheidungsphase zu integrieren, wodurch höhere Anforderungen an Genauigkeit, Sensitivität und Verfügbarkeit der Tests gestellt werden. Die beiden im Folgenden beschriebenen RT-PCR-basierten Nachweisprodukte erfüllen die technischen Anforderungen der Leitlinie präzise.
3.1 EGFR-Mutationsnachweis-Kit – Erweiterte ARMS-Technologieplattform
KerntechnologieDie verbesserte ARMS-Technologie ermöglicht die spezifische Amplifikation von seltenen Mutantensequenzen vor dem Hintergrund einer hohen Wildtyp-DNA-Konzentration.
Drei technische Sicherheitsvorkehrungen:
-Verbessertes ARMS → verbessert die Mutationserkennung
-Enzymatische Anreicherung → verdaut Wildtyp-Hintergrundsequenzen und reichert Mutantensequenzen an
-Temperaturblockierung → unterdrückt unspezifische Amplifikation
Leistung: Empfindlichkeit von1 % Mutationsfrequenz
KontaminationskontrolleEingebaute interne Kontrolle + UNG-Enzym verhindern Kontamination
BearbeitungszeitBetrieb im geschlossenen Rohr, ungefähr120 Minuten
Probenkompatibilität:Gewebe/FlüssigbiopsieBeispiele → erfüllt die Anforderung „Testen im Vorfeld“.
Abdeckung:45 Mutationenin den EGFR-Exons 18-21, die genau den in den Leitlinien hervorgehobenen Regionen entsprechen (Exon-19-Deletionen und Exon 21 L858R)
Klinische Anwendung: Steuert die EGFR-TKI-Therapie direkt.
3,2 MMT EML4-ALK Fusionsnachweis-Kit – RNA-basierte Fusionsnachweislösung

-TechnologieplattformRNA-basierte RT-PCR bietet gegenüber DNA-basierten Methoden inhärente Vorteile beim Nachweis von Genfusionen.
-RNA-basierter Vorteil: Erkennt exprimierte Fusions-Transkripte direkt und vermeidet so effektiv falsch-negative Ergebnisse
-StudienergebnisseBei ALK-Fusionen mit geringer Häufigkeit ist die RT-PCR deutlich zuverlässiger als DNA-basierte Tests.
-Empfindlichkeit: Erkennt Fusionen bis hin zu20 Kopien pro Reaktion
-Abdeckung der Varianten: Covers12 häufige EML4-ALK-Fusionsvarianten(einschließlich Variante 1 ~33 %; Varianten 3a/3b zusammen ~29 %)
-Betriebs- und KontaminationskontrolleGeschlossenes Röhrchen, ca. 120 Minuten; integrierte Prozesskontrollen + UNG-Enzym verhindern falsche Ergebnisse
-InstrumentenkompatibilitätKompatibel mit verschiedenen gängigen Echtzeit-PCR-Geräten
-Ausrichtung der Richtlinien: In hohem Maße mit der ESMO-Leitlinie vereinbar
IV. Übereinstimmung zwischen den Tests und den Empfehlungen der Leitlinie
Die beiden Nachweisprodukte stimmen in folgenden Schlüsselaspekten weitgehend mit der ESMO-Leitlinie 2025 für frühe und lokal fortgeschrittene nicht-kleinzellige Lungenkarzinome überein:
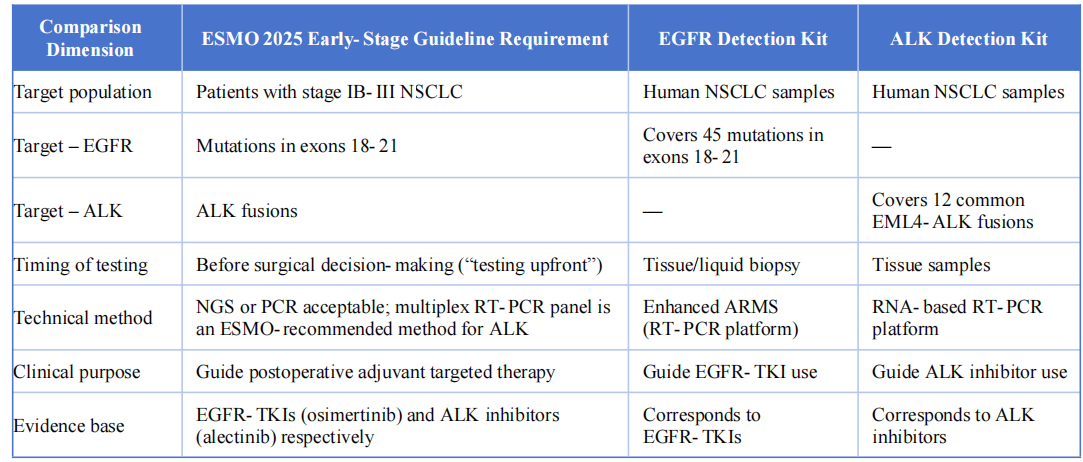
V. Schlussfolgerung
Die ESMO-Leitlinie 2025 für NSCLC im Frühstadium läutet eine neue Ära der Präzisionsdiagnostik und -therapie ein, die sich auf „Vorabtests, präzise Zielsetzung und Behandlungsoptimierung.„Das EGFR Mutation Detection Kit und das MMT EML4-ALK Fusion Detection Kit erfüllen die Anforderungen der Richtlinie hinsichtlich Zielsetzung, Zeitpunkt und Genauigkeit durch unterschiedliche technische Ansätze.“
Das EGFR-Kit nutzt die verbesserte ARMS-Technologie für den hochempfindlichen Nachweis gezielter Mutationen in begrenzten Proben und unterstützt sowohl Gewebe- als auch Flüssigbiopsien, um ein „Testing upfront“ zu ermöglichen.
Das ALK-Kit basiert auf RNA-basierter RT-PCR und bietet Vorteile gegenüber DNA-Methoden für den Fusionsnachweis. Es entspricht der ESMO-Empfehlung von Multiplex-RT-PCR-Panels für ALK-Tests.
Zusammen bilden diese beiden Produkte eine Präzisionstestlösung, die mit der ESMO-Leitlinie 2025 übereinstimmt und die personalisierte adjuvante Therapie für NSCLC im Frühstadium unterstützt.
Referenzen:
- Zer A, Ahn MJ, Barlesi F, et al. Frühes und lokal fortgeschrittenes nicht-kleinzelliges Lungenkarzinom: ESMO-Leitlinie zur klinischen Praxis für Diagnose, Behandlung und Nachsorge. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Veröffentlichungsdatum: 06.05.2026

