Der 24. März 2026 ist der 31. Welttuberkulosetag. Die Weltgesundheitsorganisation (WHO) hat das diesjährige globale Motto bekannt gegeben:„Ja! Wir können die Tuberkulose besiegen!“Er betonte, dass eine starke Führung durch die Regierung, ein nachhaltiges politisches Engagement und koordinierte sektorübergreifende Maßnahmen unerlässlich seien, um die Tuberkulose-Epidemie (TB) zu beenden.

Globale Fortschritte und verbleibende Herausforderungen
Laut dem Globalen Tuberkulosebericht 2025 erreichte die globale Tuberkulosebekämpfung im Jahr 2024 einen bedeutenden Meilenstein, wobei sowohl iInzidenz und Mortalität sinkenzum ersten Mal seit der COVID-19-Pandemie.
Eine geschätzte10,7 Millionen MenschenIm Jahr 2024 erkrankten 54 % der Menschen an Tuberkulose, 35 % der Frauen und 11 % der Kinder und Jugendlichen an Tuberkulose. Unter diesen Fällen befanden sich etwa619.000 (5,8 %)waren mit HIV koinfiziert, und390.000 (3,6 %)Es handelte sich um multiresistente oder Rifampicin-resistente Tuberkulose (MDR/RR-TB).
TB verursachte ungefähr1,23 Millionen ToteTuberkulose wird auch 2024 weltweit die häufigste Todesursache durch Infektion sein und COVID-19 übertreffen. Nach drei Jahren mit steigenden Fallzahlen zwischen 2021 und 2023 ging die weltweite Tuberkuloseinzidenz 2024 um fast 2 % zurück, was eine allmähliche Erholung der Tuberkuloseversorgung widerspiegelt.[1]
Geographisch,67 % der Fällekonzentrierten sich auf acht Länder: Indien, Indonesien, Philippinen, China, Pakistan, Nigeria, Demokratische Republik Kongo und Bangladesch.
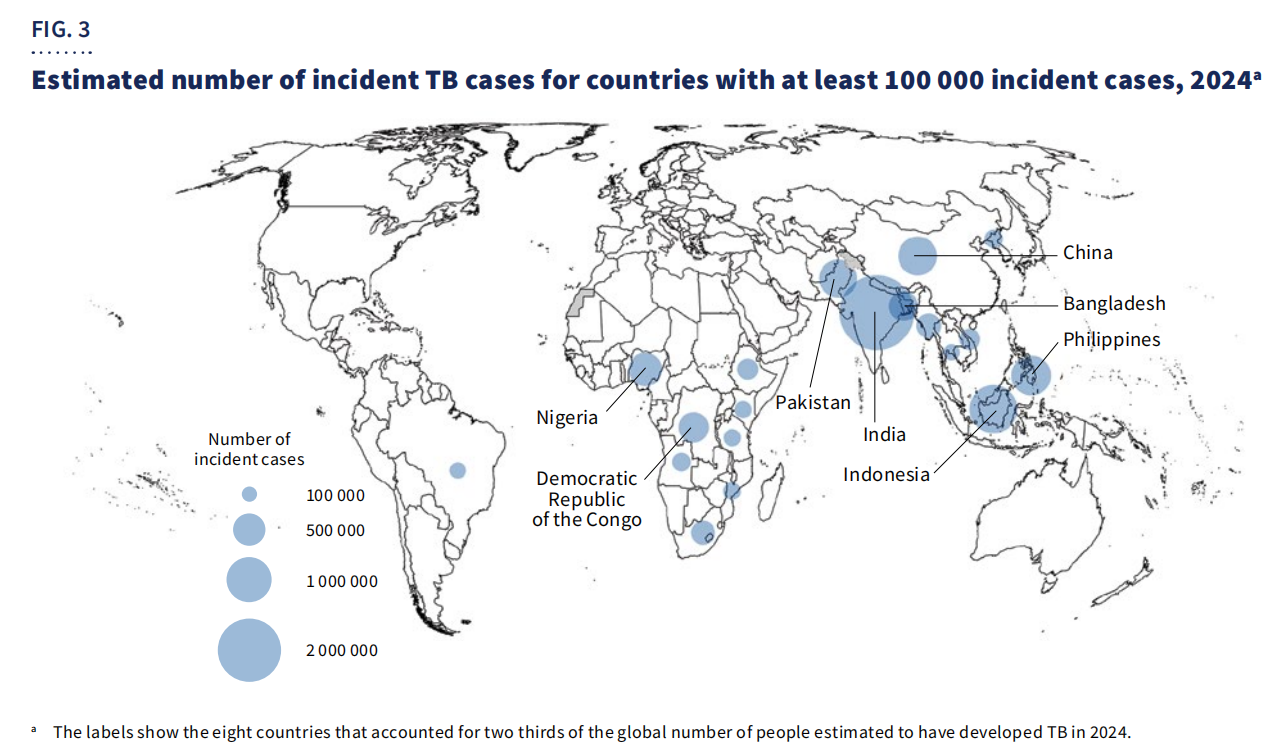
Trotz Fortschritten bleibt Tuberkulose eine der häufigsten Todesursachen bei HIV-Infizierten und trägt maßgeblich zur Sterblichkeit im Zusammenhang mit Antibiotikaresistenzen bei. Die weltweiten Finanzmittel reichen weiterhin nicht aus, da nur …5,9 Milliarden US-Dollarverfügbar ab 2024 – weit unter dem22 Milliarden US-Dollar jährliches Zielgeplant für 2027.
Diese Zahlen unterstreichen die dringende Notwendigkeit, die Tuberkulosebekämpfungsprogramme weltweit zu stärken. Dabei muss der Fokus auf dem Ausbau des Zugangs zu Diagnostik, der Verbesserung der Behandlungsergebnisse und der Bekämpfung der sozialen Faktoren liegen, die die Tuberkuloseübertragung begünstigen. Die Bekämpfung der Tuberkulose erfordert weiterhin eine enge internationale Zusammenarbeit und ein starkes politisches Engagement, um die Ziele der Strategie zur Beendigung der Tuberkulose zu erreichen.
Mycobacterium tuberculosis: Pathogenese und Klassifizierung
Mycobacterium tuberculosis (MTB/M. tuberculosis) ist der primäre und häufigste Erreger der Tuberkulose (TB). Er kann über die Atemwege, den Verdauungstrakt oder verletzte Haut und Schleimhäute in den menschlichen Körper gelangen, verschiedene Organe infizieren und unterschiedliche Formen der TB verursachen. Die Lungentuberkulose, die hauptsächlich durch Tröpfcheninfektion übertragen wird, macht über 80 % aller TB-Fälle aus. Häufige Symptome sind Husten, Auswurf und Bluthusten. Nach einer Infektion der Lunge können sich die Bakterien über die Blutbahn in verschiedene Organsysteme ausbreiten und potenziell zu Skelett-, Harnwegs- oder Magen-Darm-Tuberkulose führen. [2]
MTB gehört zur Gattung Mycobacterium, zu der auch Folgendes zählt:
- Mycobacterium tuberculosis-Komplex (MTBC): Besteht unter anderem aus M. tuberculosis, M. bovis, M. africanum, M. canettii und M. microti. Während M. tuberculosis die Hauptursache für Tuberkulose ist, können auch M. bovis und M. africanum die Krankheit auslösen.
- Nicht-tuberkulöse Mykobakterien (NTM).
- Mycobacterium leprae, der Erreger der Lepra.
Labordiagnostische Verfahren
Eine genaue und zeitnahe Diagnose ist für eine wirksame Tuberkulosebekämpfung unerlässlich. Die Weltgesundheitsorganisation betont, dassSchnelle molekulardiagnostische Verfahren haben die Tuberkulose-Erkennung grundlegend verändert, indem sie eine hochsensitive und spezifische Identifizierung von Krankheitserregern ermöglichen und gleichzeitig Arzneimittelresistenzen aufdecken.[1].
- Mikroskopie und Kulture: Die Kultur gilt weiterhin als Goldstandard für die Tuberkulosediagnostik, da sie die eindeutige Identifizierung lebensfähiger Erreger ermöglicht und die Testung der Arzneimittelempfindlichkeit sowie die Genomanalyse unterstützt. Aufgrund des langsamen Wachstums von Mycobacterium tuberculosis dauert es jedoch in der Regel 2–8 Wochen, bis die Ergebnisse vorliegen, was die klinische Anwendbarkeit bei dringenden Entscheidungen einschränkt.
-Immunologische Tests: Immunologische Methoden, darunter der Tuberkulin-Hauttest (TST) und Interferon-Gamma-Freisetzungstests (IGRA), weisen die Immunantwort des Wirts auf eine Tuberkuloseinfektion nach. Obwohl sie zur Identifizierung latenter Infektionen geeignet sind, können diese Tests nicht zuverlässig zwischen aktiver und zurückliegender Infektion unterscheiden und weisen daher in Gebieten mit hoher Tuberkuloseprävalenz eine begrenzte diagnostische Spezifität auf.
-Molekulardiagnostik (NAAT): DNA-basierte Tests wie die Nukleinsäureamplifikation (NAAT) werden aufgrund ihrer hohen Sensitivität und Spezifität empfohlen.
-Gezielte Sequenzierung der nächsten Generation (tNGS): Gezielte Sequenzierungstechnologien ermöglichen die hochauflösende Identifizierung von Resistenz-assoziierten Mutationen. Die WHO-Richtlinien empfehlen tNGS als fortschrittliches Instrument zur Erkennung von Arzneimittelresistenzen nach der Diagnose und unterstützen so präzisionsmedizinische Behandlungsstrategien [3].
-Metagenomische Sequenzierung der nächsten Generation (mNGS): Die Metagenomsequenzierung ermöglicht den unvoreingenommenen Nachweis eines breiten Spektrums an Krankheitserregern ohne vorherige Zielauswahl. Dieser Ansatz ist besonders wertvoll in komplexen oder unklaren klinischen Fällen, wie z. B. bei Mischinfektionen und immungeschwächten Patienten, bei denen herkömmliche Diagnoseverfahren möglicherweise nicht ausreichen.
Die WHO hebt außerdem hervor, dass eine mikrobiologische Bestätigung unerlässlich ist, um eine angemessene Therapie einzuleiten und die Behandlungsergebnisse für die Patienten zu verbessern, und unterstreicht damit die Bedeutung der Integration fortschrittlicher molekularer Diagnostik in Tuberkulosebekämpfungsprogramme [1].
Umfassende molekulardiagnostische Lösungen von Macro & Micro-Test
1.Multiplex-PCR-Nachweis für Tuberkulose und ArzneimittelresistenzTB
| Produktcode | Produktname | Zertifizierung |
| HWTS-RT001 | Mycobacterium Tuberculosis DNA-Nachweiskit (Fluoreszenz-PCR) | CE |
| HWTS-RT137 | Mycobacterium Tuberculosis Isoniazid-Resistenzmutations-Nachweiskit (Schmelzkurve) | CE |
| HWTS-RT074 | Mycobacterium Tuberculosis Nukleinsäure- und Rifampicin-Resistenz-Nachweiskit (Schmelzkurve) | CE |
| HWTS-RT102 | Nukleinsäure-Nachweiskit basierend auf enzymatischer Sondenisothermer Amplifikation (EPIA) für Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Gefriergetrocknetes Nukleinsäure-Nachweiskit für den Mycobacterium-tuberculosis-Komplex (Enzymatische Sonden-Isotherme Amplifikation) | CE |
| HWTS-RT105 | Kit zum Nachweis von gefriergetrockneter Mycobacterium-tuberculosis-DNA (Fluoreszenz-PCR) | CE |
| HWTS-RT147 | Mycobacterium Tuberculosis Nukleinsäure und Rifampicin, Isoniazid Resistenznachweis-Kit (Schmelzkurve) | CE |
Bei einem starken klinischen Verdacht auf Tuberkulose (TB)HWTS-RT147Der Test wird zur qualitativen Erkennung einer MTB-Infektion und multiresistenter Tuberkulose (MDR-TB) empfohlen. Dieser Test identifiziert Mutationen imrpoB-Gen, die zu Rifampicin-Resistenz (RIF) und Mutationen in derkatG- und InhA-GeneDiese sind mit einer Isoniazid(INH)-Resistenz assoziiert. Der Test ermöglicht eine effiziente Einmalanwendung sowohl für MTB als auch für MDR-TB und beinhaltet eine interne Qualitätskontrolle zur Minimierung falsch-negativer Ergebnisse, wodurch schnelle und präzise Resultate gewährleistet werden.
2.PTNseq-Zielsequenzierung für respiratorische Krankheitserreger und Resistenzprofilierung
| Produktcode | Produktname | Spezifikation. |
| HWKF-TS0001 | PTNseq-Kit zur Anreicherung von Erregergenen bei Blutstrominfektionen | 24 Tests/Kit |
| HWKF-TS0002 | PTNseq Genanreicherungskit für pathogene Mikroorganismen bei Infektionen des zentralen Nervensystems | 24 Tests/Kit |
| HWKF-TS0003 | PTNseq Kit zur Anreicherung von Genen von Erregern respiratorischer Infektionen | 24 Tests/Kit |
| HWKF-AT0003 | PTNseq Respiratory Infection Pathogenic Microorganisms Automated Enrichment Library Construction Kit (ONT) | 24 Tests/Kit |
| HWKF-TS0004 | PTNseq Breitband-Genanreicherungskit für infektiöse Krankheitserreger | 24 Tests/Kit |
| HWKF-TS0005 | PTNseq Ultra-Breitband-Genanreicherungskit für infektiöse pathogene Mikroorganismen | 24 Tests/Kit |
| HWKF-TS0151 | Kit zur Mykobakterien-Typisierung und Anreicherung von Antibiotikaresistenzgenen (Mehrfache Amplifikationsmethode) | 24 Tests/Kit |
Bei gemischten Atemwegsinfektionen (einschließlich Infektionen der oberen und unteren Atemwege, Tuberkulose und chronischen Atemwegserkrankungen) oder wenn eine Analyse von Arzneimittelresistenzgenen erforderlich ist (z. B. bei Verdacht auf arzneimittelresistente Tuberkulose),PTNseq-Serie zur gezielten Hochdurchsatz-GenanalysePTNseq basiert auf fortschrittlicher, zielgerichteter Sequenzierungstechnologie und nutzt Ultra-Multiplex-PCR zur Anreicherung spezifischer Zielsequenzen, kombiniert mit Hochdurchsatzsequenzierung und Nanoporentechnologie der dritten Generation zur umfassenden Pathogenidentifizierung und zur Erstellung von Resistenzprofilen.
Das System nutzt patentierte, hochspezifische Primer zur Ultra-Multiplex-Amplifikation von Zielgenen. Unterstützt durch eine proprietäre Datenbank und intelligente Bioinformatik-Algorithmen ermöglicht es die präzise Identifizierung von Krankheitserregern sowie die Analyse von Resistenzen und Virulenzgenen. Die gezielte Anreicherung reduziert Störungen durch Wirts-DNA, verbessert die Sensitivität in Proben mit hohem humanem Hintergrund und ermöglicht den effektiven Nachweis schwer detektierbarer Zielgene.Mycobacterium tuberculosisPilze, intrazelluläre Bakterien, RNA-Viren und Resistenz- oder Virulenzgene.
PTNseq erreicht eine Nachweisgrenzebis zu 100 Kopien/mlund deckt175 häufige Atemwegserreger, darunter 76 Bakterien, 73 Viren, 19 Pilze, 7 Mykoplasmen sowieChlamydien, Rickettsienund 54 ArzneimittelresistenzgeneDas Panel umfasst dieMycobacterium tuberculosiskomplexe und wichtige nicht-tuberkulöse Mykobakterien.
Die PTNseq-Serie vereint hohe Sensitivität mit Kosteneffizienz, verbessert die Nachweisrate von Krankheitserregern und unterstützt eine individualisierte antimikrobielle Therapie, wodurch Antibiotikaresistenzen eingedämmt werden. Integriert in das vollautomatische System zur Erstellung von Gensequenzierungsbibliotheken (AIOS) bietet sie eine optimierte Lösung für den Einsatz im Krankenhaus mit einer Bearbeitungszeit von nur 6,5 Stunden von der Probenentnahme bis zum Ergebnis.

3. Metagenomische Sequenzierung zur Erkennung eines breiten Spektrums von Krankheitserregern
| Produktcode | Produktname | Spezifikation. |
| HWKF-MN0011 | Metagenomischer Pathogennachweis-Kit (DNA-Illumina) | 24 Tests/Kit |
| HWKF-MN0018 | Metagenomischer Pathogennachweis-Kit (DNA-MGI) | 24 Tests/Kit |
| HWKF-MN0021 | Metagenomischer Pathogennachweis-Kit (DNA-ONT) | 24 Tests/Kit |
| HWKF-MN0012 | Metagenomischer Pathogennachweis-Kit (RNA-Illumina) | 24 Tests/Kit |
| HWKF-MN0019 | Metagenomischer Pathogennachweis-Kit (RNA-MGI) | 24 Tests/Kit |
| HWKF-MN0022 | Metagenomischer Pathogennachweis-Kit (RNA-ONT) | 24 Tests/Kit |
| HWKF-MN0013 | Metagenomischer Pathogennachweis-Kit (DNA+RNA-Illumina) | 24 Tests/Kit |
| HWKF-AYM0013 | Metagenomische Pathogendetektion Automatisierte Bibliothekskonstruktion Kit (DNA+RNA-Illumina) | 24 Tests/Kit |
| HWKF-MN0020 | Metagenomischer Pathogennachweis-Kit (DNA+RNA-MGI) | 24 Tests/Kit |
| HWKF-MN0023 | Metagenomisches Pathogen-Nachweiskit (DNA+RNA-ONT) | 24 Tests/Kit |
Wenn die klinische Diagnose unklar ist,mNGS-Pathogen-Hochdurchsatz-GennachweisDie Methode kann an verschiedenen Patientenproben durchgeführt werden, darunter bronchoalveoläre Lavageflüssigkeit, Sputum, Rachenabstriche, Blut, Pleuraerguss, Eiter und Gewebeproben. Dabei kommt die metagenomische Sequenzierungstechnologie zum Einsatz, bei der die verschiedenen Proben einer gezielten Vorbehandlung unterzogen werden. Anschließend erfolgt die Nukleinsäureextraktion mithilfe von Glasperlen und zellwandspaltenden Enzymen, wodurch die Extraktionseffizienz gesteigert wird. Die Sequenzierung ist an verschiedene Plattformen angepasst und gewährleistet so ein hohes Datenvolumen für eine verbesserte mNGS-Sensitivität und Assemblierungsintegrität. Die Daten werden mithilfe einer eigens entwickelten Datenbank und intelligenter Algorithmen analysiert, um …mehr als 20.000 Krankheitserreger, einschließlich Bakterien, Pilzen, Viren und Parasiten, und liefert Informationen über vermutete Krankheitserreger. Diese Methode eignet sich für schwer zu diagnostizierende, schwerkranke oder immungeschwächte Patienten, einschließlich der Identifizierung vonMTBKomplexUndNTMsowie Mischinfektionen. Es verbessert die Nachweisrate von Krankheitserregern deutlich und unterstützt den gezielten Einsatz von Antibiotika in der klinischen Praxis, wodurch eine präzise Infektionsdiagnose ermöglicht wird.
Abschluss
Obwohl beachtliche Fortschritte erzielt wurden, bleibt die Tuberkulose eine große globale gesundheitliche Herausforderung, insbesondere im Hinblick auf Arzneimittelresistenzen, Finanzierungslücken und den ungleichen Zugang zu Diagnostik.
Die WHO betont, dass der Ausbau des Zugangs zu schnellen molekularen Diagnoseverfahren und fortschrittlichen Sequenzierungstechnologien unerlässlich ist, um die Ziele der Strategie zur Beendigung der Tuberkulose zu erreichen. Dank kontinuierlicher Innovation, Investitionen und globaler Zusammenarbeit ist die Beendigung der Tuberkulose kein Wunschtraum mehr, sondern ein erreichbares Ziel.
Referenzen:
- Weltgesundheitsorganisation. Globaler Tuberkulosebericht 2024/2025: Diagnostik und Behandlung.
- Weltgesundheitsorganisation. WHO-Handbuch zur Auswahl molekularer, von der WHO empfohlener Schnelltests zur Diagnose von Tuberkulose und arzneimittelresistenter Tuberkulose.
- Weltgesundheitsorganisation. WHO-Leitlinien zur Tuberkulose: Modul 3 – Diagnose (Aktualisierung 2024).
Veröffentlichungsdatum: 24. März 2026
