Tuberkulose (TB) ist zwar vermeidbar und heilbar, stellt aber weiterhin eine globale Gesundheitsbedrohung dar. Schätzungsweise 10,6 Millionen Menschen erkrankten im Jahr 2022 an TB, was weltweit zu schätzungsweise 1,3 Millionen Todesfällen führte – weit entfernt vom Ziel der WHO-Strategie zur Beendigung der Tuberkulose bis 2025. Darüber hinaus stellt die zunehmende Resistenz gegen Tuberkulosemedikamente, insbesondere die MDR-TB (resistent gegen Rifampicin und Isoniazid), eine wachsende Herausforderung für die weltweite TB-Behandlung und -Prävention dar.
Eine effiziente und genaue Diagnose von Tuberkulose und Resistenzen gegen Tuberkulosemedikamente ist der Schlüssel zum Erfolg der Tuberkulosebehandlung und -prävention.
Unsere Lösung
Marco & Micro-Test3-in-1-Tuberkulose-Nachweis für Tuberkuloseinfektion/RIF- und NIH-ResistenzDas Nachweiskit ermöglicht die effiziente Diagnose von TB und RIF/INH in einer einzigen Untersuchung mittels Schmelzkurvenanalyse.
Die 3-in-1-TB/MDR-TB-Erkennung, die sowohl die TB-Infektion als auch die Resistenz gegen wichtige Erstlinienmedikamente (RIF/INH) bestimmt, ermöglicht eine rechtzeitige und genaue TB-Behandlung.
Die dreifache Tuberkulose-Testung (Tuberkuloseinfektion, RIF- und NIH-Resistenz) wird erfolgreich in einer einzigen Untersuchung durchgeführt!
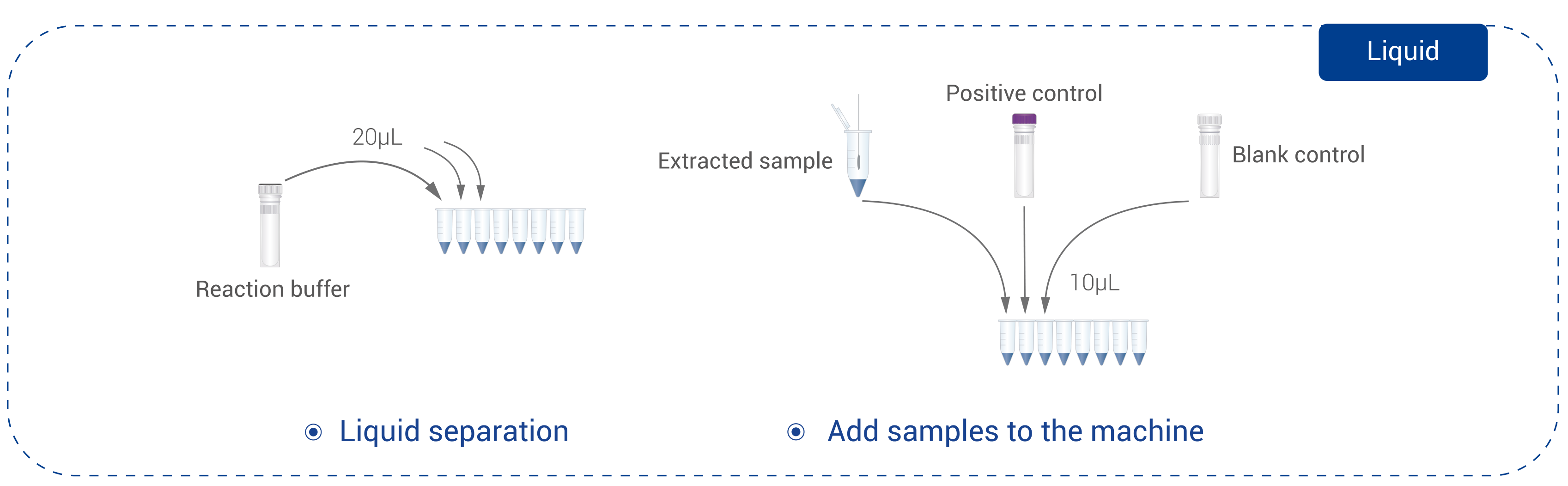
Schnelles Ergebnis:Verfügbar in 2-2,5 Stunden mit automatischer Ergebnisinterpretation, wodurch der technische Schulungsaufwand für die Bedienung minimiert wird;
Testbeispiel:Sputum, LJ-Medium, MGIT-Medium, Bronchiallavageflüssigkeit;
Hohe Empfindlichkeit:110 Bakterien/ml für TB, 150 Bakterien/ml für RIF-Resistenz, 200 Bakterien/ml für INH-Resistenz, wodurch eine zuverlässige Erkennung auch bei geringer Bakterienlast gewährleistet wird.
Mehrere Ziele:TB-IS6110; RIF-Resistenz-rpoB (507~533); INH-Resistenz-InhA, AhpC, katG 315;
Qualitätsvalidierung:Interne Kontrollmechanismen zur Validierung der Probenqualität, um falsch negative Ergebnisse zu reduzieren;
Breite Kompatibilitäty: Kompatibilität mit den meisten gängigen PCR-Systemen für eine breite Laborzugänglichkeit (SLAN-96P , BioRad CFX96);
Einhaltung der WHO-Richtlinien:Einhaltung der WHO-Richtlinien für die Behandlung von arzneimittelresistenter Tuberkulose, um Zuverlässigkeit und Relevanz in der klinischen Praxis zu gewährleisten.
Veröffentlichungsdatum: 19. September 2024
