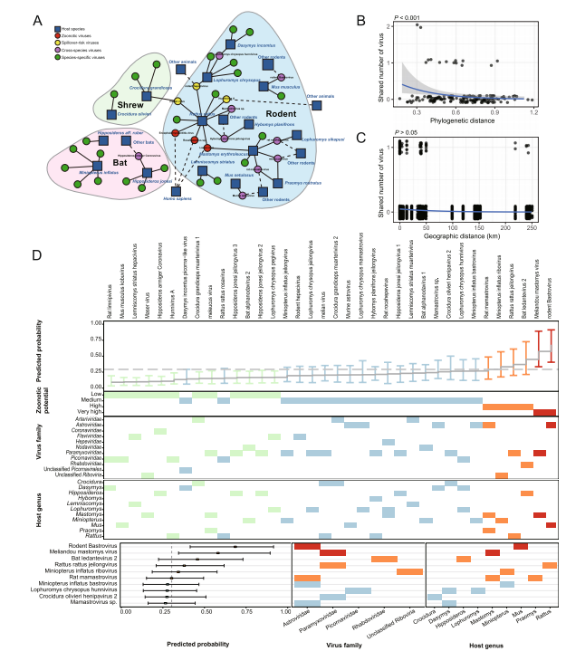
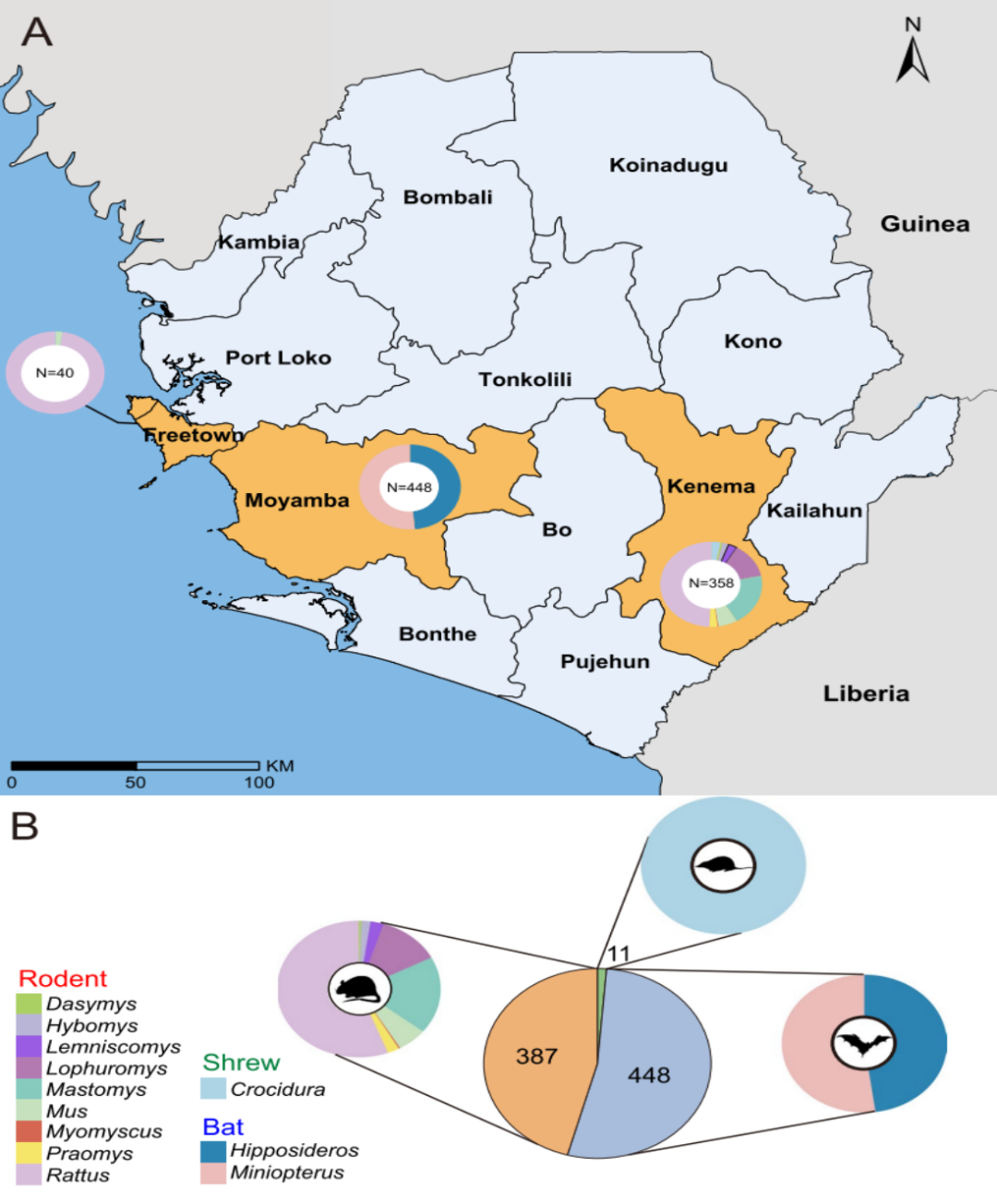
Eine kürzlich veröffentlichte StudieMikrobiomEine virale Metagenomanalyse wurde an 846 wildlebenden Kleinsäugern – darunter Fledermäuse, Nagetiere und Spitzmäuse – in Sierra Leone, Westafrika, durchgeführt. Die Studie identifizierte insgesamt 39 Säugetier-assoziierte RNA-Viren, darunter 26 neue und 13 bereits bekannte Viren. Die Familie der Paramyxoviridae wies die größte Diversität auf, während Nagetiere die größte Anzahl an Virusarten beherbergten (n = 26).
Die Zoonoserisikobewertung identifizierte drei bekannte Zoonoseviren – das Enzephalomyokarditisvirus, das Lassa-Virus und Rocahepevirus sp. – sowie drei Viren mit potenziellem Übertragungsrisiko: das Melian-Virus, das Nagetierhepatitisvirus und das Hunnivirus A. Bemerkenswerterweise wies das Fledermaus-Ledantevirus 2 unter den neu identifizierten Viren die engste phylogenetische Verwandtschaft zum humanpathogenen Le-Dantec-Virus auf. Serologische Analysen wiesen zudem neutralisierende Antikörper gegen dieses Virus bei 2,8 % der Anwohner nach, was auf eine frühere, wahrscheinlich unbemerkte Exposition beim Menschen hindeutet.
Diese Ergebnisse verdeutlichen das Vorhandensein eines bedeutenden, von Nagetieren dominierten Virusreservoirs in Westafrika und unterstreichen die entscheidende Bedeutung integrierter Überwachungsstrategien an der Schnittstelle zwischen Mensch und Tier. Die Kombination von metagenomischem Screening mit serologischer Validierung bietet einen soliden Rahmen zur Identifizierung von Viren mit zoonotischem Potenzial und Übertragungspotenzial.

Im vergangenen Jahrzehnt stammen über 60 % der neu auftretenden Infektionskrankheiten beim Menschen aus tierischen Reservoirs, wobei Fledermäuse, Nagetiere und Spitzmäuse als wichtige Wirte zoonotischer Viren gelten. Afrika wird weithin als Hotspot für Zoonosen angesehen. So wurden beispielsweise in Sierra Leone während des Ebola-Ausbruchs 2014–2016 über 28.000 Fälle gemeldet.
Trotz der erheblichen Belastung durch Zoonosen in dieser Region sind die Vielfalt und Verbreitung von Viren in wildlebenden Kleinsäugern noch unzureichend erforscht. Um diese Lücke zu schließen, führten Forschende eine systematische Viromanalyse von 846 wildlebenden Kleinsäugern durch, die zwischen 2018 und 2023 an drei Standorten in Sierra Leone gefangen wurden. Ziel der Studie war es, die virale Vielfalt zu charakterisieren, Kandidaten mit Potenzial zur Übertragung zwischen verschiedenen Arten zu identifizieren, das zoonotische Risiko zu bewerten und Daten für Frühwarnsysteme für neu auftretende Infektionskrankheiten zu generieren.
Kernmethoden
Die Studie wandte einen umfassenden Workflow der viralen Metagenomik an:
- Probenverarbeitung:Herz-, Leber-, Milz-, Lungen- und Nierengewebe wurden gesammelt, vereinigt, homogenisiert und einer Extraktion der Gesamt-RNA unterzogen.
- Sequenzierung und Assemblierung:Vor der Bibliothekspräparation wurde ribosomale RNA entfernt, gefolgt von einer Hochdurchsatzsequenzierung mit der Illumina NovaSeq 6000-Plattform. Virale Contigs wurden de novo assembliert.
- Virusidentifizierung:Die Viren wurden anhand der Sequenzanalyse des RNA-abhängigen RNA-Polymerase-Gens (RdRp) identifiziert. Es wurden nur mit Wirbeltieren assoziierte Viren berücksichtigt; bakterielle, pilzliche und pflanzliche Viren wurden ausgeschlossen.
- Bioinformatische Analyse:Es wurden phylogenetische Rekonstruktionen, Rekombinationsanalysen, Modellierungen von Übertragungsnetzwerken zwischen verschiedenen Arten und eine Bewertung des zoonotischen Risikos durchgeführt.
- Serologische Validierung:Für das Bat-Ledantevirus 2 wurde ein VSV-basierter Pseudovirus-Neutralisationstest entwickelt. Neutralisierende Antikörper wurden in 2,8 % der menschlichen Seren nachgewiesen, was einen Hinweis auf eine mögliche Zoonoseübertragung liefert.
StudieErgebnisse
1. Virale Entdeckung und Diversität
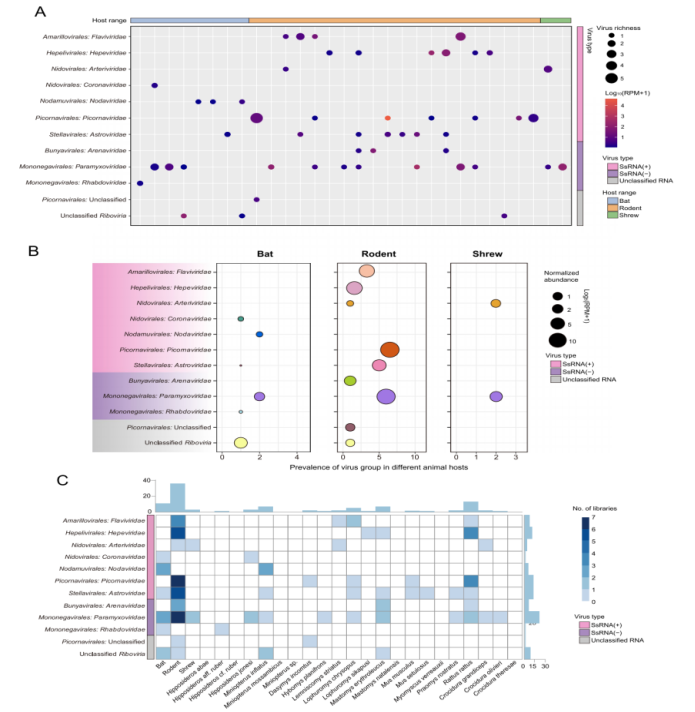
In dieser Studie wurde eine Transkriptomsequenzierungsanalyse an 846 in Sierra Leone gesammelten Wildtieren durchgeführt, darunter Nagetiere, Fledermäuse und Spitzmäuse. Basierend auf den vollständigen Sequenzen des RNA-abhängigen RNA-Polymerase-Gens (RdRp) wurden insgesamt 39 Säugetier-assoziierte RNA-Viren identifiziert, darunter 13 bereits bekannte und 26 neuartige Viren.
Hinsichtlich der Viruszusammensetzung wies die Familie der Paramyxoviridae die größte Diversität über alle drei Wirtsordnungen hinweg auf, gefolgt von den Astroviridae und Picornaviridae. Bezüglich der Wirtsverteilung trugen Nagetiere mit insgesamt 26 Virusarten am meisten zur Virusdiversität bei und spielten damit eine bedeutende Rolle als Reservoir für die Virusvielfalt in der Region.
2. Zoonotisches Risiko
Die Zoonose-Risikobewertung identifizierte drei bekannte Zoonoseviren: das Enzephalomyokarditisvirus, das Lassa-Virus und Rocahepeviren. Darüber hinaus wurden drei Viren – das Melian-Virus, das Nagetierhepatitisvirus und das Hunnivirus A – als potenziell von Zoonosen übertragbar eingestuft.
Unter den 26 neu entdeckten Viren wurde bei vieren aufgrund phylogenetischer und genomischer Merkmale ein hohes zoonotisches Potenzial vorhergesagt. Besonders hervorzuheben ist die enge phylogenetische Verwandtschaft des Fledermaus-Ledantevirus 2 mit dem bekannten, den Menschen infizierenden Le-Dantec-Virus.
Nachfolgende serologische Untersuchungen bestätigten diesen Befund, da neutralisierende Antikörper gegen das Fledermaus-Ledantevirus 2 in 2,8 % der Seren von Anwohnern nachgewiesen wurden. Dieses Ergebnis deutet darauf hin, dass unerkannte oder asymptomatische Infektionen bereits in der Bevölkerung stattgefunden haben könnten und weist auf einen potenziellen, bisher aber unbekannten Übertragungsweg für Zoonosen hin.
3. Dynamik der Übertragung zwischen verschiedenen Arten
Die Analyse der Übertragung zwischen verschiedenen Arten zeigte, dass Nagetiere eine zentrale Rolle im Netzwerk des Virusaustauschs einnehmen und als wichtige Knotenpunkte fungieren, die den Virusaustausch zwischen Wirtsarten ermöglichen. Insgesamt wurden 15 Viren identifiziert, die potenziell zur Übertragung zwischen verschiedenen Arten geeignet sind.
Weitere Analysen der Übertragungsmuster zwischen verschiedenen Ordnungen zeigten, dass der Virusaustausch häufiger zwischen Wirten derselben taxonomischen Ordnung stattfand, was darauf hindeutet, dass die Verwandtschaft der Wirte eine wichtige Rolle in der Übertragungsdynamik spielt. Fledermäuse hingegen wiesen eine relativ geringere Fähigkeit zur Übertragung zwischen verschiedenen Ordnungen auf.
Wichtig ist, dass bei bestimmten Viren Hinweise auf eine Ausweitung des Wirtsspektrums beobachtet wurden. So wurde beispielsweise das Melian-Virus, das zuvor als spezifisch für Spitzmäuse galt, in dieser Studie auch in Nagetieren nachgewiesen. Dies deutet auf eine mögliche Verschiebung der Wirtsanpassungsfähigkeit und ein erhöhtes Risiko einer breiteren Übertragung hin.
Schlussfolgerungen und Auswirkungen auf die öffentliche Gesundheit
- Hohe Viromdiversität bei wildlebenden Kleinsäugern:Die Entdeckung von 39 RNA-Viren, darunter 26 neue Arten, offenbart ein großes Virusreservoir in der Region und berichtet erstmals über neuartige Viren mit hohem zoonotischen Potenzial (z. B. Bat ledantevirus 2).
- Nagetiere als vorrangige Überwachungsziele:Nagetiere fungieren als wichtige Knotenpunkte für die Virusübertragung und weisen die höchste Virusdiversität auf, wodurch das größte Risiko einer Übertragung auf andere Viren besteht.
- Notwendigkeit integrierter Überwachungsstrategien:Die Ergebnisse sprechen dafür, Nagetiere in aktiven Überwachungsprogrammen zu priorisieren und integrierte Ansätze zu implementieren, die Metagenomik, Serologie und ökologisches Monitoring an den Schnittstellen zwischen Mensch und Wildtier kombinieren.
Insgesamt liefert diese Studie wichtige Erkenntnisse zur Unterstützung von Frühwarnsystemen und Risikobewertungsrahmen für neu auftretende Zoonosen und unterstreicht die Bedeutung einer proaktiven Überwachung in Hochrisikoregionen.
Produktinformationen
Veröffentlichungsdatum: 23. März 2026