- 1. Globale Krankheitslast durch Gebärmutterhalskrebs und Herausforderungen beim Screening
Gebärmutterhalskrebs stellt trotz seiner weitgehenden Vermeidbarkeit durch effektive Vorsorgeuntersuchungen und frühzeitige Intervention weiterhin eine große globale Herausforderung für die öffentliche Gesundheit dar. Laut Weltgesundheitsorganisation (WHO) traten im Jahr 2022 weltweit schätzungsweise 662.000 Neuerkrankungen und 349.000 Todesfälle auf. Damit ist Gebärmutterhalskrebs die vierthäufigste Krebsart und die vierthäufigste krebsbedingte Todesursache bei Frauen. Die Krankheitslast konzentriert sich unverhältnismäßig stark auf Länder mit niedrigem und mittlerem Einkommen (LMICs), wo die Inzidenz- und Mortalitätsraten deutlich höher sind als in Ländern mit hohem Einkommen. Dies ist vor allem auf einen Mangel an qualitativ hochwertigen Vorsorgeprogrammen sowie an effizienter Erkennung und Behandlung von Krebsvorstufen zurückzuführen, verstärkt durch:
-Fehlende oder schwache Screening-InfrastrukturMangel an zugänglichen, qualitätsgesicherten Screening-Dienstleistungen.
-Ressourcenbeschränkungen: Begrenzte Laborinfrastruktur, Kühlkettenlogistik und zuverlässige Stromversorgung.
-Arbeitskräftemangel: Mangel an geschultem Labor- und Klinikpersonal.
-Verzögerungen und Verlust der Nachbeobachtung: Verzögerung zwischen Probenentnahme und Verfügbarkeit der Ergebnisse, was zu Verzögerungen in der klinischen Behandlung oder zum Verlust von Patienten für die Nachbeobachtung führt[1].
2. Ätiologie und molekulare Grundlagen der Zervixkarzinogenese
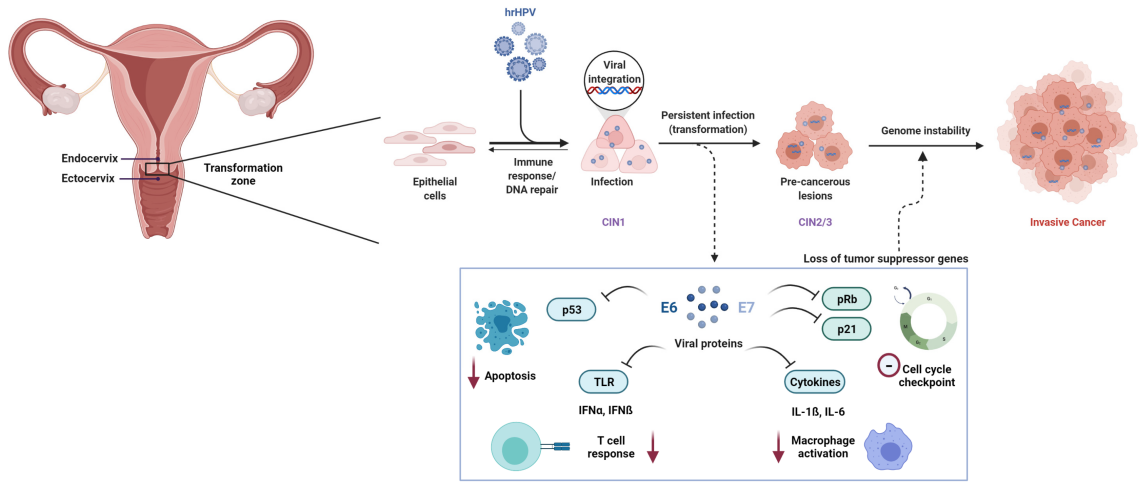
Eine persistierende Infektion mit Hochrisiko-Humanpapillomaviren (HR-HPV) ist eine notwendige Ursache für Gebärmutterhalskrebs. Von den mehr als 200 identifizierten HPV-Genotypen sind mindestens12 Typenwurden von der Internationalen Agentur für Krebsforschung (IARC) als krebserregend (Gruppe 1) eingestuft.

Auf molekularer Ebene wird die HPV-vermittelte Karzinogenese primär durch die viralen Onkoproteine E6 und E7 angetrieben. E6 fördert den Abbau des Tumorsuppressorproteins p53, während E7 das Retinoblastomprotein (Rb) funktionell inaktiviert, was zu einer Dysregulation des Zellzyklus und zur malignen Transformation führt.
3.Von der WHO empfohlene Screening-Strategien
Die Weltgesundheitsorganisation empfiehlt den HPV-Nukleinsäuretest (NAT) als bevorzugte primäre Screening-Methode zur Vorbeugung von Gebärmutterhalskrebs.
Allgemeine Bevölkerung:HPV-DNA- oder mRNA-basierte NATs
Frauen, die mit HIV leben:HPV-DNA-basierte NATs
Screeningintervalle:
Frauen im Alter von 30–65 Jahren: Alle 5–10 Jahre
Frauen mit HIV: Alle 3–5 Jahre
Im Vergleich zu zytologischen Methoden zeigt der HPV-Test Folgendes:höhere Empfindlichkeitund bieteteinen überlegenen negativen Vorhersagewertwodurch längere und kostengünstigere Screening-Intervalle ermöglicht werden.
4.WHO-Zielproduktprofil für HPV-Screeningtests
Die WHO hat einZielproduktprofil (TPP)für HPV-Screeningtests, die für den Einsatz in dezentralen und ressourcenbeschränkten Umgebungen vorgesehen sind.[1]
Zu den wichtigsten Merkmalen gehören:
- Kompatibilität mit selbst gesammelten Proben
- Nachweis mehrerer Hochrisiko-HPV-Genotypen (≥12 Typen)
- Bedienung durch nicht laborgeschultes Personal
- Ergebnisse liegen bereits nach einer einzigen Arztkonsultation vor.
Diese Kriterien unterstützen patientennahe Tests und „Screening-and-Treat“-Strategien.
5.Eine vollautomatische Plattform zur Erkennung von Hochrisiko-HPV.
Das AIO800-System von Macro & Micro-Test bietetein vollautomatisierter Workflow von der Probe bis zur AntwortIntegration von Nukleinsäureextraktion, -amplifikation und -nachweis gemäß den von der WHO empfohlenen Screening-Strategien.

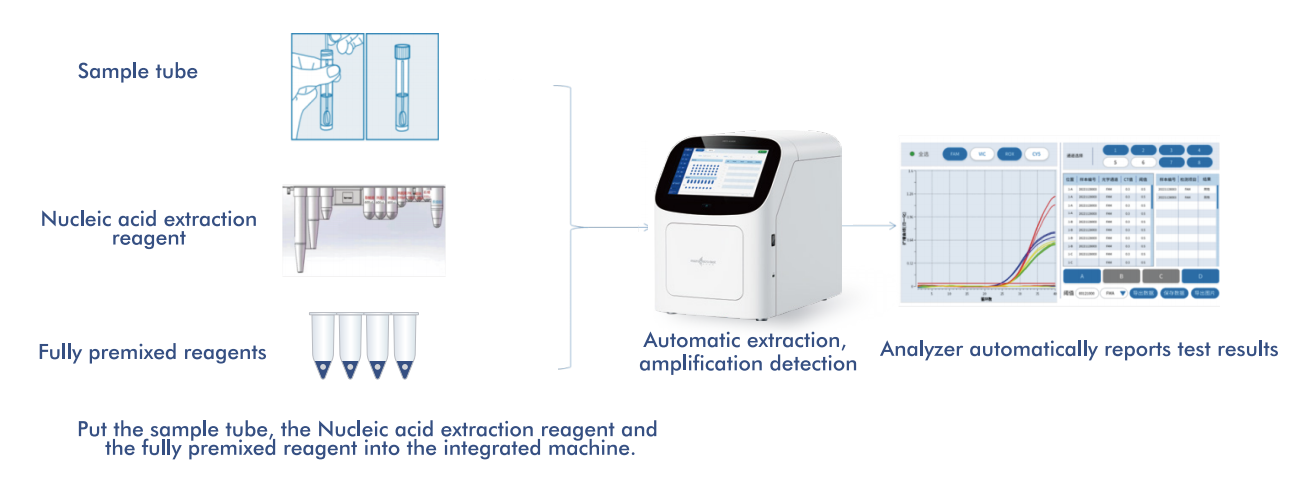
5.1 Automatisierter Workflow von der Probe bis zur Antwort
Die Plattform integriert Nukleinsäureextraktion, -amplifikation und -detektion in einem einzigen, geschlossenen System und erfordert nur minimalen Bedienereingriff. Dieses Design:
- -Verringert die Abhängigkeit von spezialisiertem Laborpersonal
- - Minimiert Prozessvariabilität und Kontaminationsrisiko
- - Ermöglicht den Einsatz in dezentralen Gesundheitseinrichtungen
Gleichzeitig ermöglicht die hohe Durchsatzkapazität den Einsatz in zentralisierten Laboren und erleichtert so groß angelegte Screening-Programme.
5.2 Umfassende Genotypisierungsabdeckung
Das System erkennt 14 Hochrisiko-HPV-Typen, darunter alle 12 von der IARC klassifizierten krebserregenden Typen (HPV16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 und 59) sowie HPV66 und HPV68.
Wichtig ist, dass es Folgendes bietettypenspezifische GenotypisierungErgebnisse, die eine Risikostratifizierung und ein präziseres klinisches Management ermöglichen.
5.3 Analytische Sensitivität und klinische Implikationen
Mit einer Nachweisgrenze von 300 Kopien/ml ist das System in der Lage, geringgradige HPV-Infektionen zu erkennen, die zu Folgendem beitragen:
- -Frühere Erkennung klinisch relevanter Infektionen
- -Verbesserter negativer Vorhersagewert
- -Unterstützung verlängerter Screening-Intervalle
5.4 Unterstützung für Selbstprobenahme
Die Plattform ist mit beiden kompatibelZervixabstrichproben und selbst entnommene Urinprobenin Übereinstimmung mit den Empfehlungen der WHO zur Beseitigung wichtiger Hindernisse für die Inanspruchnahme von Vorsorgeuntersuchungen, einschließlich:
- -Eingeschränkter Zugang zu Gesundheitseinrichtungen
- -Soziokulturelle Zwänge
Veröffentlichungsdatum: 27. März 2026
