Jedes Jahr am 17. April ist Weltkrebstag.
01 Weltweite Übersicht über die Krebsinzidenz
In den letzten Jahren hat mit dem stetigen Anstieg des Lebens- und psychischen Drucks der Menschen auch die Häufigkeit von Tumoren von Jahr zu Jahr zugenommen.
Bösartige Tumore (Krebs) haben sich zu einem der größten Gesundheitsprobleme entwickelt und bedrohen die Gesundheit der chinesischen Bevölkerung ernsthaft. Laut aktuellen Statistiken sind 23,91 % aller Todesfälle in China auf bösartige Tumore zurückzuführen, und die Häufigkeit und die Todesfälle durch bösartige Tumore sind in den letzten zehn Jahren stetig gestiegen. Doch Krebs ist kein Todesurteil. Die Weltgesundheitsorganisation (WHO) betont, dass bei frühzeitiger Erkennung 60–90 % der Krebserkrankungen heilbar sind! Ein Drittel aller Krebserkrankungen ist vermeidbar, ein Drittel heilbar und ein Drittel kann lebensverlängernd behandelt werden.
02 Was ist ein Tumor?
Ein Tumor ist ein neuer Organismus, der durch die Proliferation lokaler Gewebezellen unter dem Einfluss verschiedener tumorfördernder Faktoren entsteht. Studien haben gezeigt, dass Tumorzellen andere Stoffwechselveränderungen durchlaufen als normale Zellen. Gleichzeitig können sich Tumorzellen an Veränderungen im Stoffwechselmilieu anpassen, indem sie zwischen Glykolyse und oxidativer Phosphorylierung wechseln.
03 Individualisierte Krebstherapie
Die individualisierte Krebstherapie basiert auf der Diagnose von Zielgenen und den Ergebnissen evidenzbasierter medizinischer Forschung. Sie bildet die Grundlage für die individuelle Anpassung der Behandlung und ist damit zum Trend der modernen Medizin geworden. Klinische Studien haben bestätigt, dass die Analyse von Genmutationen und Biomarkern, die Bestimmung von SNP-Typen sowie die Analyse des Gen- und Proteinexpressionsstatus in biologischen Proben von Tumorpatienten die Vorhersage der Wirksamkeit von Medikamenten, die Prognosebewertung und die Steuerung der individualisierten Therapie verbessern, Nebenwirkungen reduzieren und den rationalen Einsatz medizinischer Ressourcen fördern.
Die molekulare Diagnostik von Krebs lässt sich in drei Haupttypen unterteilen: diagnostische, hereditäre und therapeutische Tests. Therapeutische Tests bilden den Kern der sogenannten „therapeutischen Pathologie“ oder personalisierten Medizin. Immer mehr Antikörper und niedermolekulare Inhibitoren, die tumorspezifische Schlüsselgene und Signalwege gezielt angreifen, finden Anwendung in der Tumortherapie.
Die molekular gezielte Tumortherapie zielt auf Markermoleküle von Tumorzellen ab und greift in deren Entwicklungsprozess ein. Ihre Wirkung beschränkt sich hauptsächlich auf Tumorzellen, während normale Zellen nur geringfügig beeinträchtigt werden. Tumorwachstumsfaktorrezeptoren, Signaltransduktionsmoleküle, Zellzyklusproteine, Apoptoseregulatoren, proteolytische Enzyme, vaskulärer endothelialer Wachstumsfaktor usw. können als molekulare Zielstrukturen für die Tumortherapie dienen. Die am 28. Dezember 2020 von der Nationalen Gesundheits- und Medizinischen Kommission veröffentlichten „Verwaltungsmaßnahmen für die klinische Anwendung von Antineoplastika (Studie)“ legen klar fest: Bei Arzneimitteln mit eindeutigen Genzielen muss das Anwendungsprinzip nach einer Testung der Zielgene befolgt werden.
04 Tumorgerichtete Gentests
Tumoren weisen vielfältige genetische Mutationen auf, die jeweils unterschiedliche zielgerichtete Medikamente erfordern. Nur durch die genaue Bestimmung der Mutationsart und die Auswahl der passenden Therapie können Patienten einen Nutzen erzielen. Molekulare Nachweismethoden wurden eingesetzt, um die Variationen von Genen, die mit häufig eingesetzten Medikamenten in Zusammenhang stehen, in Tumoren zu erfassen. Die Analyse des Einflusses genetischer Varianten auf die Wirksamkeit der Medikamente unterstützt Ärzte bei der Entwicklung eines optimalen, individuellen Behandlungsplans.
Lösung 05
Macro & Micro-Test hat eine Reihe von Nachweiskits für den Tumorgennachweis entwickelt und bietet damit eine Gesamtlösung für die zielgerichtete Tumortherapie.
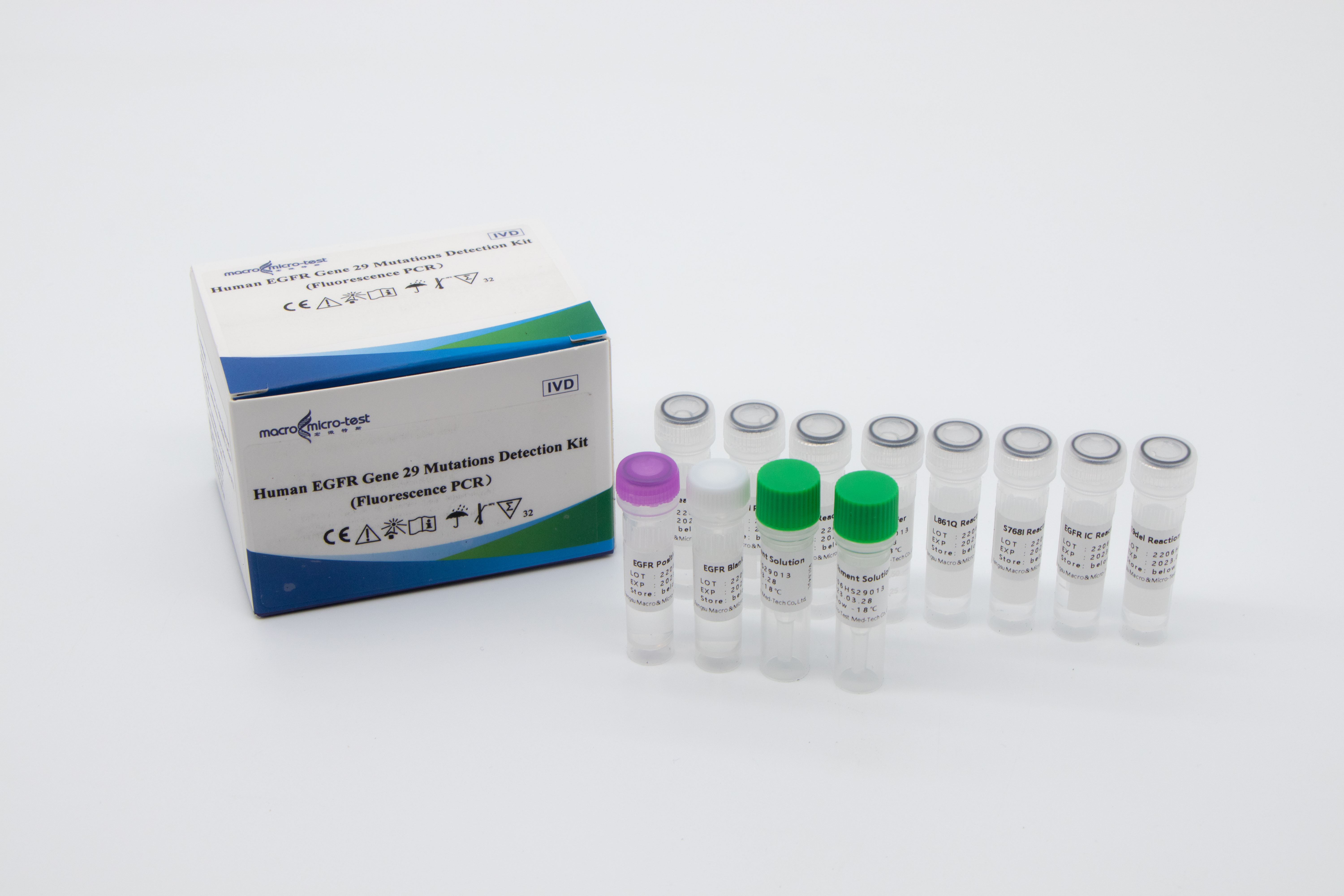
Kit zum Nachweis von 29 Mutationen des menschlichen EGFR-Gens (Fluoreszenz-PCR)
Dieses Kit dient dem qualitativen In-vitro-Nachweis häufiger Mutationen in den Exons 18-21 des EGFR-Gens in Proben von Patienten mit nicht-kleinzelligem Lungenkrebs.
1. Das System führt eine interne Referenzqualitätskontrolle ein, die den experimentellen Prozess umfassend überwachen und die Qualität des Experiments sicherstellen kann.
2. Hohe Empfindlichkeit: Die Detektion der Nukleinsäure-Reaktionslösung kann eine Mutationsrate von 1 % vor dem Hintergrund von 3 ng/μL Wildtyp stabil nachweisen.
3. Hohe Spezifität: Keine Kreuzreaktion mit humaner Wildtyp-Genom-DNA und anderen Mutanten.
 |  |
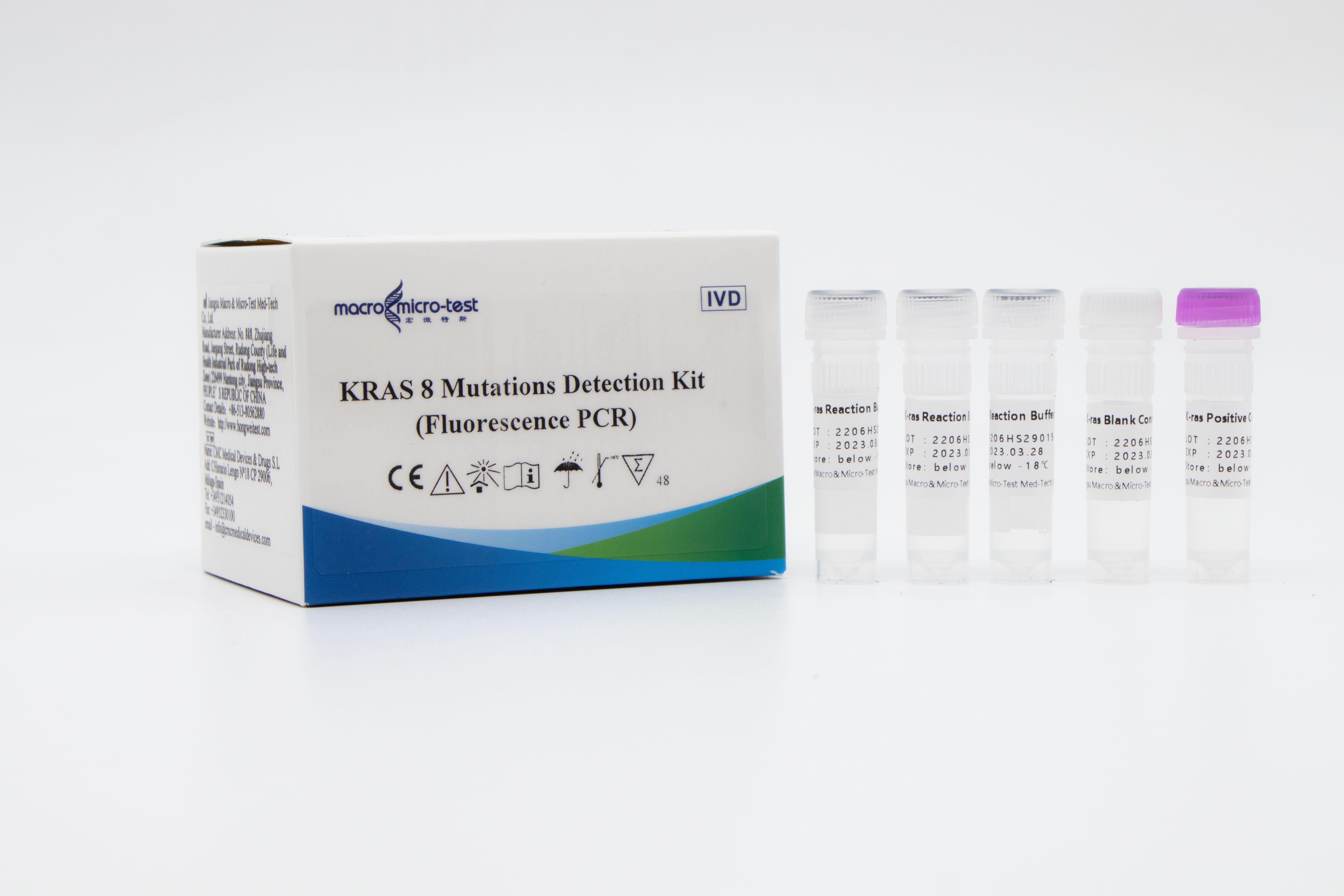
KRAS 8 Mutationsnachweis-Kit (Fluoreszenz-PCR)
Dieses Kit ist für den qualitativen In-vitro-Nachweis von 8 Mutationen in den Codons 12 und 13 des K-ras-Gens in extrahierter DNA aus menschlichen, in Paraffin eingebetteten pathologischen Schnitten bestimmt.
1. Das System führt eine interne Referenzqualitätskontrolle ein, die den experimentellen Prozess umfassend überwachen und die Qualität des Experiments sicherstellen kann.
2. Hohe Empfindlichkeit: Die Detektion der Nukleinsäure-Reaktionslösung kann eine Mutationsrate von 1 % vor dem Hintergrund von 3 ng/μL Wildtyp stabil nachweisen.
3. Hohe Spezifität: Keine Kreuzreaktion mit humaner Wildtyp-Genom-DNA und anderen Mutanten.
 |  |
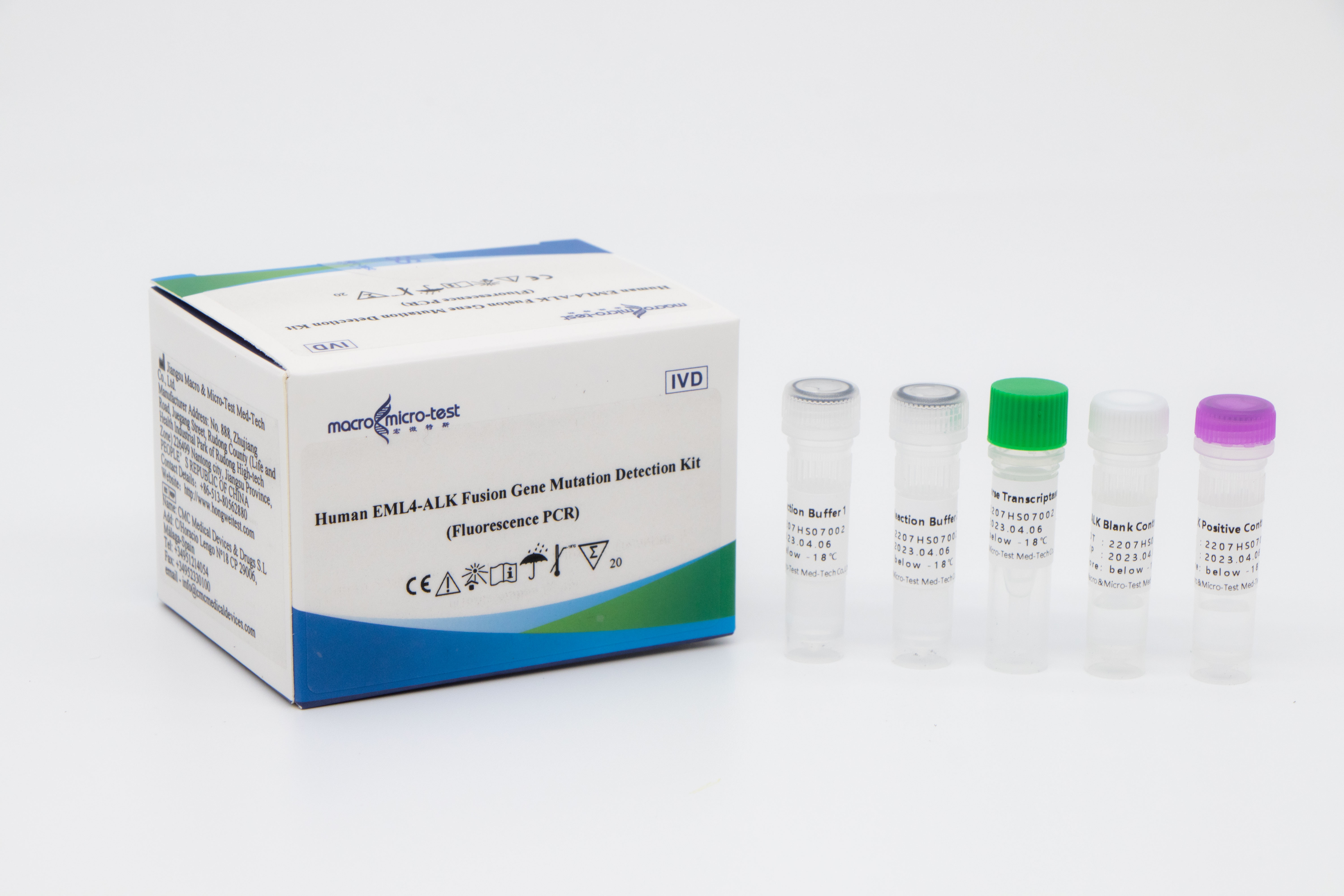
Kit zum Nachweis von Mutationen des humanen EML4-ALK-Fusionsgens (Fluoreszenz-PCR)
Dieses Kit dient dem qualitativen Nachweis von 12 Mutationstypen des EML4-ALK-Fusionsgens in Proben von Patienten mit nicht-kleinzelligem Lungenkrebs in vitro.
1. Das System führt eine interne Referenzqualitätskontrolle ein, die den experimentellen Prozess umfassend überwachen und die Qualität des Experiments sicherstellen kann.
2. Hohe Sensitivität: Mit diesem Kit lassen sich Fusionsmutationen bereits ab 20 Kopien nachweisen.
3. Hohe Spezifität: Keine Kreuzreaktion mit humaner Wildtyp-Genom-DNA und anderen Mutanten.
 |  |
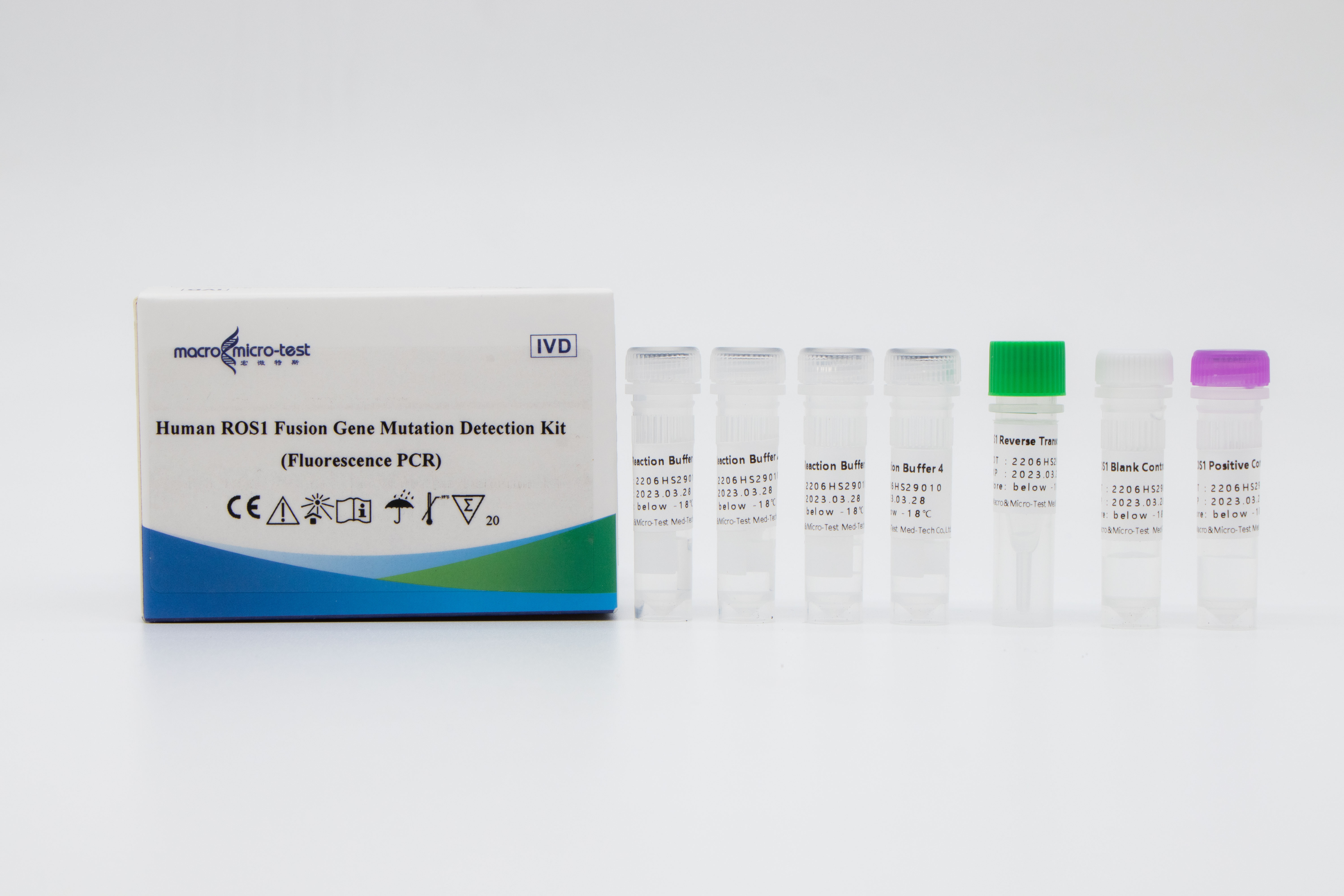
Kit zum Nachweis von Mutationen des humanen ROS1-Fusionsgens (Fluoreszenz-PCR)
Dieses Kit dient dem qualitativen In-vitro-Nachweis von 14 verschiedenen ROS1-Fusionsgenmutationen in Proben von nicht-kleinzelligem Lungenkrebs des Menschen.
1. Das System führt eine interne Referenzqualitätskontrolle ein, die den experimentellen Prozess umfassend überwachen und die Qualität des Experiments sicherstellen kann.
2. Hohe Sensitivität: Mit diesem Kit lassen sich Fusionsmutationen bereits ab 20 Kopien nachweisen.
3. Hohe Spezifität: Keine Kreuzreaktion mit humaner Wildtyp-Genom-DNA und anderen Mutanten.
 |  |
Kit zum Nachweis der humanen BRAF-Genmutation V600E (Fluoreszenz-PCR)
Mit diesem Testkit kann die BRAF-Genmutation V600E in Paraffin-eingebetteten Gewebeproben von menschlichem Melanom, Darmkrebs, Schilddrüsenkrebs und Lungenkrebs in vitro qualitativ nachgewiesen werden.
1. Das System führt eine interne Referenzqualitätskontrolle ein, die den experimentellen Prozess umfassend überwachen und die Qualität des Experiments sicherstellen kann.
2. Hohe Empfindlichkeit: Die Detektion der Nukleinsäure-Reaktionslösung kann eine Mutationsrate von 1 % vor dem Hintergrund von 3 ng/μL Wildtyp stabil nachweisen.
3. Hohe Spezifität: Keine Kreuzreaktion mit humaner Wildtyp-Genom-DNA und anderen Mutanten.
 |  |
| Katalognummer | Produktname | Spezifikation |
| HWTS-TM012A/B | Kit zum Nachweis von Mutationen des menschlichen EGFR-Gens (Fluoreszenz-PCR) | 16 Tests/Kit, 32 Tests/Kit |
| HWTS-TM014A/B | KRAS 8 Mutationsnachweis-Kit (Fluoreszenz-PCR) | 24 Tests/Kit, 48 Tests/Kit |
| HWTS-TM006A/B | Kit zum Nachweis von Mutationen des humanen EML4-ALK-Fusionsgens (Fluoreszenz-PCR) | 20 Tests/Kit, 50 Tests/Kit |
| HWTS-TM009A/B | Kit zum Nachweis von Mutationen des humanen ROS1-Fusionsgens (Fluoreszenz-PCR) | 20 Tests/Kit, 50 Tests/Kit |
| HWTS-TM007A/B | Kit zum Nachweis der BRAF-Genmutation V600E beim Menschen (Fluoreszenz-PCR) | 24 Tests/Kit, 48 Tests/Kit |
| HWTS-GE010A | Kit zum Nachweis von Mutationen des humanen BCR-ABL-Fusionsgens (Fluoreszenz-PCR) | 24 Tests/Kit |
Veröffentlichungsdatum: 17. April 2023
