1. Hintergrund der Dengue-Epidemie: Eine zunehmende globale Herausforderung für die öffentliche Gesundheit
Denguefieber ist eine akute, durch Mücken übertragene Viruserkrankung, die durch das Dengue-Virus (DENV) verursacht wird. Sie hat sich weltweit zur am schnellsten verbreitenden Arbovirus-Erkrankung entwickelt und stellt eine erhebliche Bedrohung für die öffentliche Gesundheit dar. In den letzten zwei Jahrzehnten ist die weltweite Inzidenz von Denguefieber dramatisch angestiegen; die Zahl der gemeldeten Fälle hat sich seit 2021 jährlich verdoppelt [1]. Im Dezember 2023 rief die Weltgesundheitsorganisation (WHO) einen globalen Dengue-Notstand aus, um die koordinierten internationalen Maßnahmen zu verstärken. Epidemiologische Schätzungen der WHO gehen davon aus, dass weltweit etwa 3,9 Milliarden Menschen von einer Denguefieber-Infektion bedroht sind. Schätzungsweise 390 Millionen Infektionen treten jährlich auf, davon verlaufen 96 Millionen klinisch manifest [1,2].
2 Epidemiologische Highlights
Die epidemiologischen Merkmale von Denguefieber werden durch das Zusammenspiel virologischer Faktoren, der Ökologie der Überträger, der Immunantwort des Wirts und sozioökologischer Bedingungen geprägt. Ein umfassendes Verständnis dieser Merkmale ist unerlässlich für die Entwicklung wirksamer Präventions- und Bekämpfungsstrategien sowie präziser Diagnoseverfahren.
2.1 Übertragungswege und urbane Übertragungsmuster
Das Dengue-Virus wird hauptsächlich übertragen durchAedes aegypti und Aedes albopictusMücken. Unter diesen Vektorarten gilt Aedes aegypti als der wichtigste Überträger, charakterisiert durch eine hohe Anpassungsfähigkeit an den Menschen und eine weite Verbreitung in tropischen und subtropischen städtischen Gebieten. Im Gegensatz zu anderen Mücken, die Arboviren übertragen, weist Aedes aegypti die folgenden wichtigen epidemiologischen Merkmale auf:
-Eine Vorliebe für die Brut in anthropogenen Umgebungen (z. B. Wasserspeicherbehälter, ausrangierte Reifen)
-Eine starke Affinität zu menschlichem Blut als Nährstoffquelle
- Fressverhalten am Tag
Diese Merkmale definieren Dengue als typische„urbane Infektionskrankheiten“Die Übertragungseffizienz ist in dicht besiedelten Gebieten deutlich erhöht. Studien der WHO haben gezeigt, dass in städtischen Gebieten mit hoher Bevölkerungsdichte eine erhöhte Häufigkeit des Kontakts zwischen Mücken und Menschen die Basisreproduktionszahl (R₀) des Dengue-Virus erheblich steigern und dadurch die Ausbreitung von Epidemien beschleunigen kann [2].
2.2 Globale Ausbreitungstrends und treibende Faktoren
Laut Berichten der WHO hat die weltweite Zahl der gemeldeten Dengue-Fälle in den letzten zwei Jahrzehnten exponentiell zugenommen [1,3]. Dieser Aufwärtstrend wird hauptsächlich durch folgende, miteinander verbundene Faktoren verursacht:
(1) Klimawandel: Steigende globale Temperaturen erweitern nicht nur das Verbreitungsgebiet geeigneter Lebensräume für Stechmücken als Krankheitsüberträger, sondern verkürzen auch die extrinsische Inkubationszeit des Dengue-Virus (DENV) im Stechmückenwirt und erhöhen dadurch die Übertragungseffizienz. Klimabedingte Schwankungen der Stechmückendichte wurden von der WHO als zuverlässiger Indikator für die räumlich-zeitliche Dynamik von Dengue-Ausbrüchen bestätigt.
(2) Urbanisierung: Die rasche und ungeplante Ausdehnung der Städte hat zahlreiche Brutstätten für Mückenvektoren geschaffen, während die erhöhte Bevölkerungsdichte die Kontinuität der DENV-Übertragungsketten verstärkt hat.
(3) Globale Bevölkerungsbewegungen: Internationaler Reise- und Warenverkehr haben die rasche grenzüberschreitende Ausbreitung des Dengue-Virus (DENV) begünstigt und den Übergang von importierten Fällen zu einer anhaltenden lokalen Übertragung gefördert. Daten der WHO-Überwachung zeigen, dass die Vereinigten Staaten zwischen 2010 und 2021 7.528 reisebedingte Dengue-Fälle meldeten, von denen 3.135 eine stationäre Behandlung erforderten und 19 zum Tod führten.
(4) Ausbreitung der Vektoren: Weltweit dehnt sich das Verbreitungsgebiet von Aedes aegypti und Aedes albopictus kontinuierlich aus, wobei sich Aedes-Mücken zunehmend in Teilen Europas etablieren. Infolgedessen hat sich Dengue von einer ursprünglich regionalen Epidemie zu einer globalen Bedrohung der öffentlichen Gesundheit entwickelt.
2.3 Ko-Zirkulation und Reinfektionsmechanismen mehrerer Serotypen
Das Dengue-Virus umfasst vier antigenetisch unterschiedliche Serotypen (DENV-1 bis DENV-4). Eine Infektion mit einem Serotyp verleiht eine langfristige Schutzimmunität gegen diesen spezifischen Serotyp, jedoch nur einen vorübergehenden und partiellen Kreuzschutz gegen die anderen drei Serotypen. Die Allgemeinbevölkerung ist grundsätzlich für DENV empfänglich, wobei nur ein Teil der Infizierten klinische Symptome entwickelt [2].
In endemischen Gebieten zirkulieren häufig mehrere DENV-Serotypen gleichzeitig, sodass Einzelpersonen im Laufe ihres Lebens potenziell mehrfach an Denguefieber erkranken können. Epidemiologische Studien der WHO haben die gleichzeitige Zirkulation mehrerer Serotypen als einen Hauptfaktor für periodische Dengue-Ausbrüche identifiziert [1].
2.4 Sekundärinfektion und antikörperabhängige Verstärkung
Ein entscheidendes und einzigartiges Phänomen in der Dengue-Epidemiologie istAntikörperabhängige Verstärkung (ADE)Bei einer Sekundärinfektion mit einem heterologen DENV-Serotyp erleichtern nicht-neutralisierende Antikörper, die während der Primärinfektion gebildet wurden, das Eindringen des Virus in Monozyten und Makrophagen und verstärken so die Virusreplikation. Dieser Mechanismus ist von der WHO weithin als wichtiger pathogenetischer Faktor bei schwerem Denguefieber, einschließlich hämorrhagischem Denguefieber und Dengue-Schock-Syndrom, anerkannt [1].
Epidemiologische Daten der WHO zeigen übereinstimmend, dass Personen mit einer Sekundärinfektion mit Denguefieber ein deutlich höheres Risiko für einen schweren Krankheitsverlauf aufweisen als Personen mit einer Primärinfektion – eine Eigenschaft, die für die Krankheitsüberwachung und die klinische Behandlung von großer Bedeutung ist. Es ist wichtig zu beachten, dass das Risiko eines schweren Krankheitsverlaufs zwar bei einer Sekundärinfektion erhöht ist, eine Infektion mit jedem DENV-Serotyp jedoch potenziell zu schwerem Denguefieber führen kann [1].
2.5 Risiko unspezifischer klinischer Manifestationen und Fehldiagnosen
Die klinischen Symptome von Denguefieber sind, insbesondere im Frühstadium der Erkrankung, ausgesprochen unspezifisch und ähneln häufig denen anderer durch Mücken übertragener Virusinfektionen (z. B. Chikungunya- und Zika-Virus) sowie bestimmter Atemwegsinfektionen. Schätzungen der WHO zufolge verlaufen 40–80 % der Dengue-Virus-Infektionen asymptomatisch [3].
Typische klinische Manifestationen sind:
-Akutes Fieber (das 2-7 Tage anhält und biphasisch verlaufen kann)
-Starke Kopfschmerzen und Schmerzen hinter den Augen
-Muskel- und Gelenkschmerzen (allgemein als „Knochenbruchfieber“ bezeichnet)
-Makulärer oder makulopapulöser Ausschlag
-Leichte hämorrhagische Manifestationen (z. B. Hämatome, Nasenbluten, Zahnfleischbluten)
Symptomatisches Denguefieber verläuft typischerweise in drei Phasen: die Fieberphase, die kritische Phase und die Erholungsphase. Ungefähr 5 % der symptomatischen Patienten entwickeln ein schweres Denguefieber. Aufgrund fehlender spezifischer klinischer Merkmale ist die Diagnose allein anhand der Symptome schwierig, was das Risiko von Fehldiagnosen und Unterdiagnosen erhöht. Die WHO betont ausdrücklich, dass eine klinische Diagnose allein nicht ausreicht, um eine genaue Diagnose zu gewährleisten, weshalb eine Laborbestätigung unerlässlich ist [1].
3 Kernpunkte aus dem WHO-Bericht „Labortests auf das Dengue-Virus: Vorläufige Leitlinien, April 2025“
Im April 2025 veröffentlichte die Weltgesundheitsorganisation (WHO) aktualisierte vorläufige Leitlinien für Labortests auf das Dengue-Virus (DENV) und lieferte damit maßgebliche technische Empfehlungen für die weltweite Dengue-Diagnostik. Diese Leitlinien fassen die neuesten Erkenntnisse zu Labortests auf Dengue im Kontext der anhaltenden globalen Dengue-Notlage zusammen und bieten praxisnahe Empfehlungen, die auf unterschiedliche Ressourcen zugeschnitten sind.

3.1 Grundprinzipien der Teststrategie
Die Leitlinie betont, dass die Dengue-Diagnostik eine kombinierte Teststrategie mit mehreren Markern auf Grundlage des Krankheitsstadiums anwenden muss [1]. Da es keinen universellen Diagnosealgorithmus gibt, sollten die Teststrategien an die lokalen epidemiologischen Gegebenheiten angepasst werden, wobei folgende Schlüsselfaktoren zu berücksichtigen sind [1]:
-Infektionsstadium: Die Anzahl der Tage nach Symptombeginn bestimmt die am besten geeignete Testmethode
-Probenart: Die Eignung von Vollblut, Plasma oder Serum für den DENV-Nachweis
-Regionale Epidemiologie: Die lokal zirkulierenden DENV-Serotypen und die gleichzeitige Zirkulation anderer Arboviren
-Koinfektionsrisiko: In Regionen mit sich überschneidender Arbovirus-Zirkulation sollten Multiplex-Tests in Betracht gezogen werden, um zwischen verschiedenen Krankheitserregern zu unterscheiden.
3.2 Stufenbasierte Teststrategie
Gemäß den Richtlinien der WHO sollten Dengue-Labortests in klar definierten Zeitfenstern durchgeführt werden, die sich nach dem Stadium der Erkrankung richten [1,2]:
(1) Testung in der Akutphase (≤7 Tage nach Symptombeginn)
-Nukleinsäuretest (Molekularbiologischer Test): Mittels reverser Transkriptions-Polymerase-Kettenreaktion (RT-PCR) und anderer molekularer Methoden kann DENV-RNA mit hoher Sensitivität nachgewiesen werden.
-Antigentest: Nachweis des NS1-Antigens, das innerhalb von 1-3 Tagen nach Krankheitsbeginn nachweisbar ist.
Während der akuten Phase sind die Virämiewerte relativ hoch, und Nukleinsäure- und Antigentests erreichen eine optimale Sensitivität.
(2) Testung in der Rekonvaleszenzphase (≥4 Tage nach Krankheitsbeginn)
-Serologische Tests: IgM-Antikörper sind typischerweise etwa ab dem vierten Tag nach Krankheitsbeginn nachweisbar.
In den meisten Fällen persistieren IgM-Antikörper 14 bis 20 Tage lang, in einigen Fällen kann die Persistenz bis zu 90 Tage andauern.
-IgG-Tests haben nur einen begrenzten Wert für die Diagnose von akutem Denguefieber, da es zu Kreuzreaktionen mit Antikörpern aus einer früheren Flavivirusinfektion oder -impfung kommen kann.
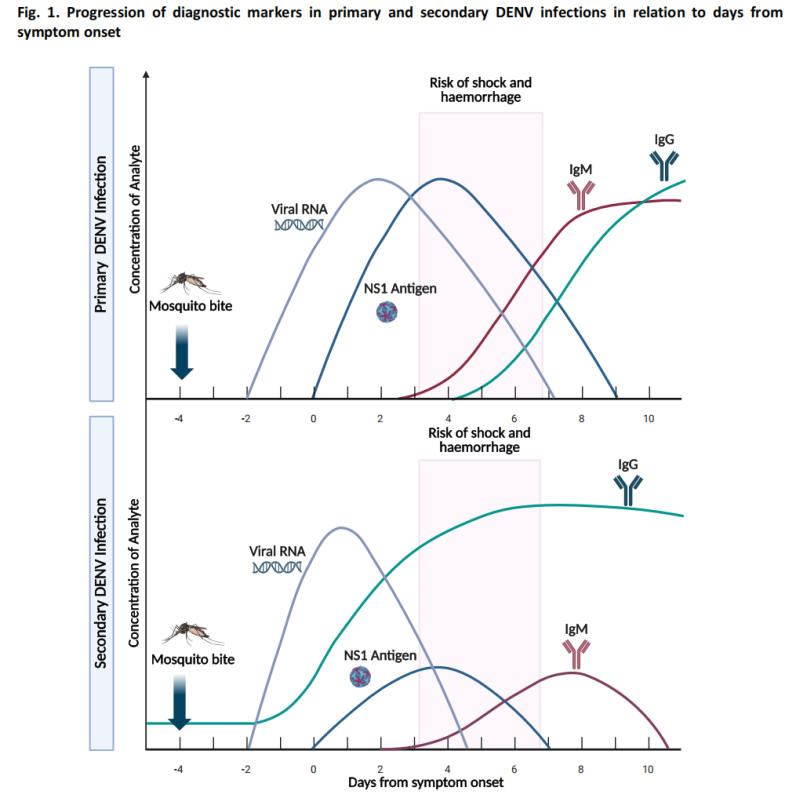
(3) Diagnosealgorithmus für Verdachtsfälle
Die Leitlinien enthalten einen Diagnosealgorithmus für Verdachtsfälle von Denguefieber und empfehlen geeignete Testmethoden je nach Anzahl der Tage nach Symptombeginn: NS1-Antigentests und Nukleinsäuretests sind die primären Ansätze in der Frühphase, während serologische Tests die primäre Methode in der späteren Phase darstellen.
3.3 Leistungsbewertung und Auswahl von Testmethoden
Laut WHO ergibt sich eine systematische Bewertung der Leistungsfähigkeit und der Anwendungsszenarien verschiedener Dengue-Tests wie folgt:
| Prüfverfahren | Ziel | Zeitfenster | Primäres Anwendungsszenario | Überlegungen |
| Nukleinsäuretest | Virale RNA | 1-7 Tage nach Beginn | Frühe Bestätigung, Serotypenidentifizierung | Goldstandard-Methode; erfordert spezielle Laborausrüstung und technisches Fachwissen |
| NS1-Antigentest | Nichtstrukturelles Protein | 1-3 Tage nach Beginn | Frühes Schnellscreening | Verfügbar als Schnelltest (RDT), geeignet für ressourcenarme Umgebungen |
| IgM-Antikörpertest | Spezifische IgM-Antikörper | ≥4 Tage nach Beginn | Diagnose einer kürzlich erfolgten Infektion | Eine einzelne Serumprobe deutet lediglich auf eine mögliche kürzlich erfolgte Infektion hin; zur Bestätigung ist eine Serokonversion erforderlich. |
| IgG-Antikörpertest | Spezifische IgG-Antikörper | Genesungsphase/vorherige Infektion | Epidemiologische Untersuchung, Beurteilung des Immunitätsstatus | Eine einzelne Serumprobe ist für die Diagnose von akutem Denguefieber nicht geeignet. |
| Kombinierter Test (NS1+IgM/IgG) | Antigen + Antikörper | Vollständiger Krankheitsverlauf | Umfassende Diagnose einer Dengue-Infektion | Das derzeit leistungsstärkste RDT-Format für die Dengue-Diagnostik |
| NGS | Virale RNA | 1-7 Tage nach Beginn | virale Genomüberwachung | Erfordert spezielle Sequenzierungsgeräte und bioinformatische Analysefähigkeiten. |
4 Produktempfehlungen für den Dengue-Nachweis mittels Makro- und Mikrotests nach Szenario
Zur Unterstützung der Dengue-Prävention und -Bekämpfung bietet Macro & Micro-Test ein integriertes Diagnostikportfolio an, das Schnelltests, molekulare Bestätigung und genomische Überwachung umfasst und somit den Bedürfnissen in verschiedenen Phasen des Ausbruchsmanagements gerecht wird.
4.1 Szenario 1: Schnellscreening und gezielte Überwachung
Anwendbar auf Fieberambulanzen, Einrichtungen der Primärversorgung, Screening-Maßnahmen bei Ausbrüchen und Quarantänemaßnahmen an Häfen/Grenzen.
-Dengue-Virus NS1-Antigen-Schnelltest: Erkennt eine frühe Infektion (1-3 Tage nach Symptombeginn) und liefert Ergebnisse in 15 Minuten für eine schnelle Triage.
-Dengue-Virus-IgM/IgG-Antikörpertest: Unterscheidet zwischen Primär- und Sekundärinfektionen zur Beurteilung des Risikos einer schweren Erkrankung.
-Dengue-Virus NS1-Antigen + IgM/IgG Kombinierter Schnelltest: Erkennt gleichzeitig Antigen und Antikörper für eine vollständige Diagnose.
-Chikungunya-Virus-IgM/IgG-Antikörpertest: Ermöglicht die Differenzialdiagnose gegenüber Denguefieber zur genauen Identifizierung von Krankheitserregern.
4.2 Szenario 2: Präzisionsdiagnose und Notfallreaktion
-Dengue-Virus I/II/III/IV Nukleinsäure-Nachweiskit: Erkennt und differenziert 4 Serotypen (Nachweisgrenze 500 Kopien/ml) zur Ausbruchsverfolgung.
-Lyophilisiertes Dengue-Virus-PCR-Kit: Bei Raumtemperatur transportierbar, geeignet für ressourcenarme Gebiete und plötzliche Ausbrüche.
-Dengue/Zika/Chikungunya Multiplex Real-Time PCR Kit: Erkennt gleichzeitig 3 Arboviren für eine effiziente Differenzialdiagnose bei komplexen Ausbrüchen.

Alle oben genannten Reagenzien sind mit dem vollautomatischen Probenanalysesystem AIO 800 kompatibel, wodurch manuelle Arbeitsschritte und Kreuzkontaminationen reduziert und die Effizienz sowie die Biosicherheit verbessert werden.
4.3 Szenario 3: Genomische Überwachung und Analyse viraler Linien
Anwendbar auf nationale Referenzlaboratorien und öffentliche Gesundheitsforschungseinrichtungen, im Einklang mit der Positionierung der WHO zu NGS.
Die Genomüberwachungslösungen von Macro & Micro-Test unterstützen die Sequenzierung des gesamten Genoms zur Virusverfolgung, Aufklärung von Übertragungsketten, Variantenüberwachung und Anpassung von Impfstrategien. Sie unterstützen manuelle und automatisierte Arbeitsabläufe, verbessern den Durchsatz und die Reproduzierbarkeit und ermöglichen Laboren den Umstieg von Routineuntersuchungen auf eine erweiterte Überwachung – ganz im Sinne der WHO-Empfehlung zur Stärkung der Überwachung der Virusentwicklung.

4.4 Wert integrierter Lösungen
Macro & Micro-Test bietet umfassende Diagnostiklösungen zum Nachweis von Arboviren und unterstützt damit jede Phase des Ausbruchsmanagements: Schnelltests für den Einsatz im Gesundheitswesen, molekulare Bestätigung für präzise Diagnosen und Genomanalysen für die epidemiologische Überwachung. Dank leistungsstarker Assays, flexibler Arbeitsabläufe und automatisierungsfähiger Plattformen ermöglichen diese Lösungen Laboren und öffentlichen Gesundheitseinrichtungen, ihre Vorsorge und Reaktion auf neu auftretende Arbovirus-Bedrohungen weltweit zu verbessern.
Referenzen
[1] Weltgesundheitsorganisation. Labortests auf das Dengue-Virus: Vorläufige Leitlinien, April 2025. Genf: Weltgesundheitsorganisation; 2025.
[2] Technische Beratungsgruppe der WHO-Initiative zur Bekämpfung globaler Arboviren. Stärkung der globalen Vorsorge und Reaktion auf Bedrohungen durch Arbovirus-Erkrankungen: Ein Aufruf zum Handeln. Lancet Infect Dis. 2026;26(1):15-17.
[3] The Lancet Microbe. Überwindung des Dilemmas der Dengue-Diagnostik. Lancet Microbe. 2025;6(7):101190.
Veröffentlichungsdatum: 20. März 2026
